Просмотр содержимого документа
«Презентация урока по развитию функциональной грамотности: "Реакции обмена"»

« Три пути ведут к знанию: путь размышления - это самый благородный; путь подражания - это путь самый лёгкий и путь опыта - это путь самый горький» Конфуций

- 37(1) 4(2) 7(1) 14(1) 40(1) 39(2) 4(4)
- 5(2) 5(1) 13(4) 16(2) 12(4) 13(1)

Реакции обмена

- На урок пришли мы дружно
- Что же здесь узнать нам нужно?

- Суть реакции обмена
- Всем умело объяснять!
- Уметь писать все уравнения
- И предвидеть, что писать!

1 вариант А) 2C + O 2 = 1) 2CO
2) CO 2
Б) 2H 2 + O 2 = 3) H 2 O 2
4) 2H 2 O
2 вариант В) 2Fe + 3Cl 2 = 5) 2FeCl 2
6) 2FeCl 3
г) 4 Na+ O 2 = 7) 2Na 2 O
8 ) Na 2 O


- 1 вариант
- 1 А) 2C + O 2 = 2CO
- 1 Б) 2H 2 + O 2 = 2H 2 O
- 2 вариант
- 2 В) 2Fe + 3Cl 2 = 2H 2 O
- 2 г) 2Na+ O 2 = 2Na 2 O
Нет ошибок – отметка «5»
1 ошибка – отметка «4»
2 ошибки – отметка «3»

- Реакции обмена - это такие реакции, в результате которых два сложных вещества обмениваются своими составными частями.
2NaI + Pb(NO3)2 = Pb I2 ↓ + 2Na NO3

- NaHCO3 + HCI = NaCI + H2O + CO2↑
- H 2 CO 3
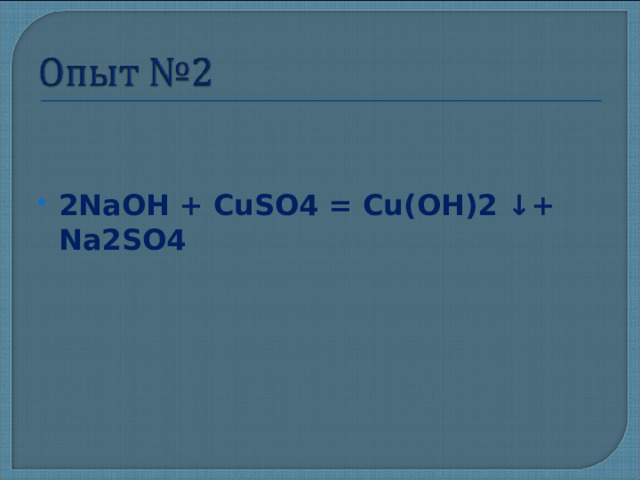
- 2NaOH + CuSO4 = Cu(OH)2 ↓+ Na2SO4

-
- NaOH + HCI = NaCI + H 2 O

- Если выделится газ - Это раз; И получится вода - Это два; А еще - нерастворимый Осаждается продукт… "Есть осадок " - говорим мы. Это третий важный пункт. Химик правила обмена Не забудет никогда: В результате - непременно Будет газ или вода , Выпадет осадок - Вот тогда - порядок!
-

Какие из реакций обмена будут протекать до конца?
- 1) BaCl2 + 2AgNO3→Ba(NO3)2+2AgCI↓
2) Cu(NO3)2 + 2NaCl→CuCI2+2NaNO3
- 3) Pb(NO3)2 + K2S→PbS↓+2KNO3
4) KOH+H2S →H2O+K2S
- 5) HCI+ K 2 S→H 2 S↑+KCI
- 6) MgCl2 + K2SO4→MgSO4+KCL
- 7) H3PO4→Ca3(PO4)2↓+6HNO3

- Составьте сиквейн: образуется, вступают, вещества, осадок, газ, вода, понравились, образуется, сложные, опыты, реакции обмена

- Прочитать §34
- Выполнить тренировочные задания естественнонаучной грамотности на сайте РЭШ к уроку 7

Сейчас прозвенит долгожданный звонок.
Увы, но к концу подошел наш урок.
Прошу, уберите рабочее место.
Давайте без слов, и пожалуй, без жестов.
А я благодарность вам всем объявляю,
Проверив работы, в журнал выставляю
Отметки все ваши, надеюсь привычно
Что будут они «хорошо» и «отлично»
Большое спасибо я вам говорю
Мы цели достигли. Благодарю!










































