
Классификация химических реакций
Реакции, идущие без изменения состава вещества
Химия – 11
Автор: Кунова Г.В. – учитель химии ГОАОУ ЦОРиО г. Липецк
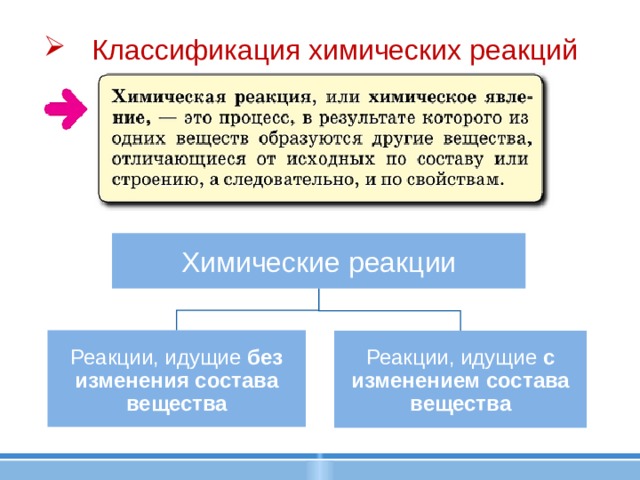
- Классификация химических реакций
Химические реакции
Реакции, идущие без изменения состава вещества
Реакции, идущие с изменением состава вещества

- Реакции, которые не сопровождаются изменением состава веществ.
- Это реакции, в результате которых из одних веществ образуются другие вещества, отличающиеся по строению и по свойствам, но одинаковые по составу .
- В неорганической химии к данной группе реакций относятся взаимопревращения аллотропных модификаций одного химического элемента .
- В органической химии - это явление изомерии .

- Взаимопревращения аллотропных модификаций одного химического элемента
- Аллотропными мoдификaциями , или видоизменениями, называют простые вещества , образованные одним химическим элементом , а явление их существования называют аллотропией.
Примеры:
- Аллотропные модификации серы :
S 8 (ромбическая) S(пластическая)
При комнатной температуре устойчива ромбическая сера. При нагревании она плавится, превращаясь в желтую легкоподвижную жидкость, при дальнейшем нагревании жидкость загустевает, так как в ней образуются длинные полимерные цепочки, а если вылить расплавленную серу в холодную воду, получится пластическая сера – резиноподобная структура.
Пластическая сера, представляющая собой аморфное вещество , через некоторое время превращается в кристаллическую ромбическую серу с молекулярной решёткой.

- Для наиболее известных аллотропных модификаций фосфора взаимопревращения можно отразить следующей схемой:
Р(белый) Р(красный)
атомная
кристаллическая
решётка,
формула P
молекулярная
кристаллическая
решётка,
формула P 4
Порошок красно-бурого цвета, неядовит, нелетуч, нерастворим в воде и во многих органических растворителях; не воспламеняется на воздухе и не светится в темноте.
Сильный яд, при температуре выше 15°C – мягкий, легко режется ножом; в воде нерастворим, легко плавится, летуч, светится в темноте.
Исторически первым осуществил превращение белого фосфора в красный немецкий алхимик Х. Брандт в 1669 г.
Получить из красного фосфора белый можно в лабораторных условиях.

- Взаимопревращение аллотропных модификаций олова:
Sn(белое) Sn(cepoe)
мягкий пластичный металл
порошок, имеющий все свойства неметаллов
Именно взаимопревращение аллотропных модификаций олова стало причиной гибели экспедиции Р. Скотта, пытавшегося в 1912 г. покорить Южный полюс.
Экспедиция Р. Скотта использовала для хранения продуктов и керосина железные канистры, запаянные оловом. На сильном морозе оловянный припой рассыпался, и экспедиция осталась без топлива.
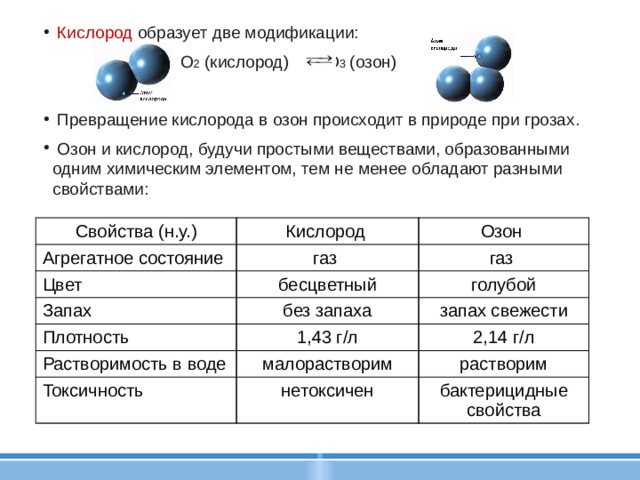
- Кислород образует две модификации:
О 2 (кислород) О 3 (озон)
- Превращение кислорода в озон происходит в природе при грозах.
- Озон и кислород, будучи простыми веществами, образованными одним химическим элементом, тем не менее обладают разными свойствами:
Свойства (н.у.)
Агрегатное состояние
Кислород
Озон
газ
Цвет
газ
Запах
бесцветный
Плотность
голубой
без запаха
Растворимость в воде
1,43 г/л
запах свежести
2,14 г/л
малорастворим
Токсичность
растворим
нетоксичен
бактерицидные свойства

Вывод
- Одной из причин многообразия неорганических веществ является аллотропия, которая может быть обусловлена:
- различным составом молекул простых веществ.
Пример: аллотропия кислорода – кислород O 2 и озон O 3 ;
2) различным кристаллическим строением аллотропных модификаций.
Пример:
все модификации углерода имеют атомную кристаллическую решётку ,
но у алмаза она — объёмная тетраэдрическая,
а у графита — слоистая,
потому так непохожи свойства алмаза и графита.

- В органической химии также известны реакции, которые протекают без изменения состава веществ.
- Такие реакции приводят к образованию изомеров.
Реакции изомеризации – это реакции взаимопревращения изомеров.
Изомеры — это вещества, имеющие одинаковый состав , т.е. одинаковую молекулярную формулу, но разное строение , а следовательно, и разные свойства.
Явление существования изомеров называют изомерией.
Изомерия — одна из причин многообразия органических соединений.
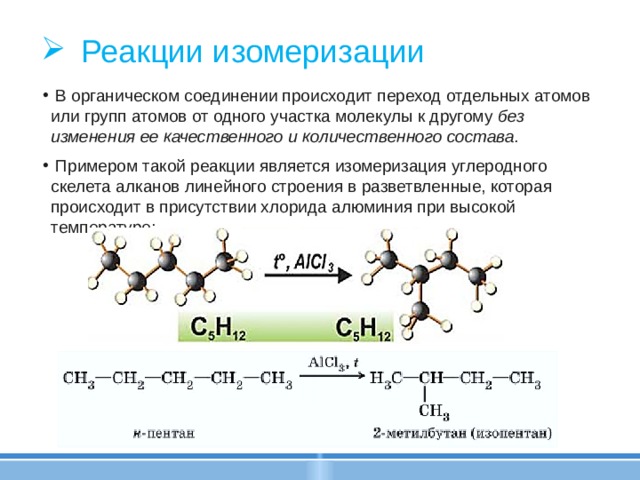
- В органическом соединении происходит переход отдельных атомов или групп атомов от одного участка молекулы к другому без изменения ее качественного и количественного состава.
- Примером такой реакции является изомеризация углеродного скелета алканов линейного строения в разветвленные, которая происходит в присутствии хлорида алюминия при высокой температуре:


Источники:





































