
Основные положения молекулярно-кинетической теории
Молекулярная физика. Тепловые явления

Все вещества имеют дискретное строение (состоят из мельчайших частиц — атомов, молекул и ионов).

Молекулярно-кинетическая теория строения вещества (МКТ) —
теория, которая объясняет строение и свойства тел движением и взаимодействием частиц, из которых состоят тела.
Даниил Бернулли
1700—1782

Основные положения молекулярно-кинетической теории
Корпускулярно-кинетическая
теория тепла —
все вещества состоят из корпускул — молекул, которые являются «собраниями» элементов — атомов, участвующих во внутреннем вращательном («коловратном») движении.
Михаил Ломоносов
1711—1765

Первое положение молекулярно-кинетической теории:
все вещества состоят из мельчайших частиц (молекул, атомов и ионов), разделённых между собой промежутками.
Основные положения МКТ
Молекула —
мельчайшая частица вещества, сохраняющая его химические, но не сохраняющая физические свойства.
Основные положения МКТ
Атом —
это мельчайшая частица химического элемента, сохраняющая его химические свойства.

Второе положение молекулярно-кинетической теории:
частицы вещества находятся в непрерывном хаотическом (тепловом) движении.

Третье положение молекулярно-кинетической теории:
частицы в веществе связаны друг с другом силами молекулярного взаимодействия.

Основные положения МКТ
Диффузия —
самопроизвольное взаимное проникновение молекул соприкасающихся веществ.
Остатки сверхновой (проявление диффузии в газах)
10

Основные положения МКТ
Атомная единица массы
(1 а. е. м.) —
это 1/12 массы атома чистого изотопа .
10

Основные положения МКТ
Относительная молекулярная (атомная) масса вещества —
величина, показывающая, во сколько раз масса молекулы (атома) больше атомной единицы массы.
10

Задача 1. Определите массу молекулы серной кислоты, химическая формула которой Н 2 SО 4 .
РЕШЕНИЕ
Относительная атомная масса водорода:
Относительная атомная масса серы:
Относительная атомная масса кислорода:
Относительная атомная масса H 2 SO 4 :
Масса молекулы H 2 SO 4 :
ОТВЕТ: масса молекулы H 2 SO 4 равна 1,6 ∙ 10 –25 кг.
10

Один моль —
количество вещества, в котором содержится столько же молекул или атомов, сколько атомов содержится в углероде массой 12 г.
10
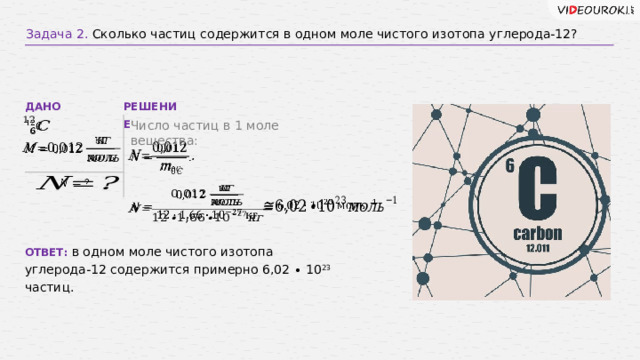
Задача 2. Сколько частиц содержится в одном моле чистого изотопа углерода-12?
РЕШЕНИЕ
ДАНО
Число частиц в 1 моле вещества:
ОТВЕТ: в одном моле чистого изотопа углерода-12 содержится примерно 6,02 ∙ 10 23 частиц.
10

Число (постоянная) Авогадро —
физическая величина, численно равная количеству частиц в 1 моле любого вещества.
Амедео Авогадро
1776—1856
10

Количество вещества —
физическая величина, характери-зующая количество частиц (молекул, атомов, ионов и пр.), содержащихся в веществе.
10
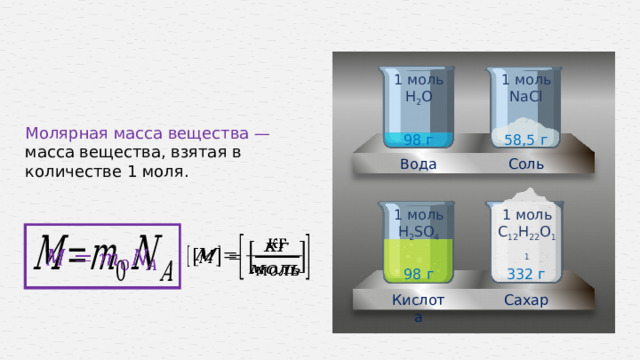
1 моль NaCl
1 моль Н 2 О
Молярная масса вещества —
масса вещества, взятая в количестве 1 моля.
58,5 г
98 г
Вода
Соль
1 моль Н 2 SО 4
1 моль C 12 Н 22 О 11
332 г
98 г
Кислота
Сахар
10
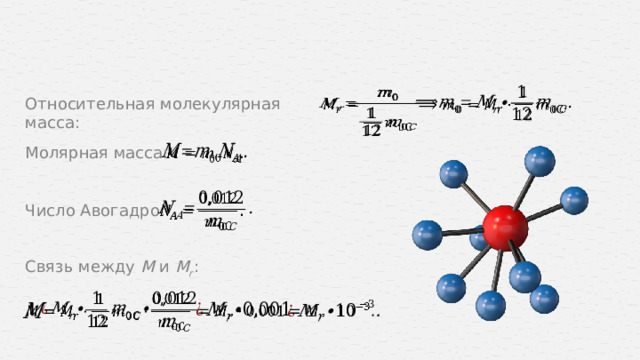
Относительная молекулярная масса:
Молярная масса:
Число Авогадро:
Связь между M и M r :
10

Масса тела —
величина, численно равная произведению массы одной молекулы вещества, из которого состоит тело, на число молекул в теле.
10
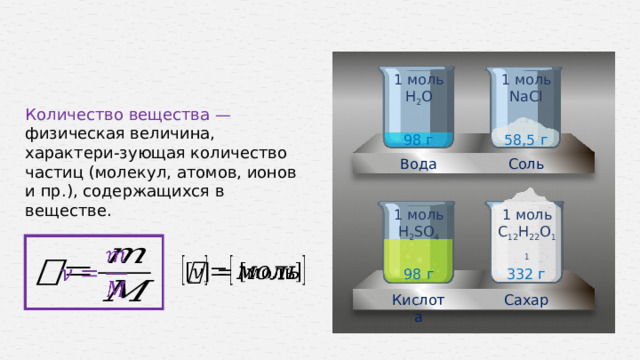
1 моль NaCl
1 моль Н 2 О
Количество вещества —
физическая величина, характери-зующая количество частиц (молекул, атомов, ионов и пр.), содержащихся в веществе.
58,5 г
98 г
Вода
Соль
1 моль Н 2 SО 4
1 моль C 12 Н 22 О 11
332 г
98 г
Кислота
Сахар
10

Задача 3. Оцените диаметр молекулы воды, если плотность воды равна 1000 кг/м 3 .
РЕШЕНИЕ
ДАНО
Молярная масса воды:
Объём, приходящийся в среднем на одну молекулу:
Количество вещества:
Объём воды:
ОТВЕТ: диаметр молекулы воды примерно равен 3,85 ∙ 10 –10 м.
10















































