Просмотр содержимого документа
«Органикалык эмес бирикмелердин классификациясы»

Органикалык эмес бирикмелердин классификациясы
Химия 8-класс

Жөнөкөй заттар
- Асыл газдар Rn , Xe, Kr, Ar, Ne, He
- Металлдар Li, Rb, K, Cs, Ba, Ca, Na, Mg, Al, Mn2+, Zn, Cr3+, Fe2+, Ni, Sn, Pb, Fe3+, | H2, | Cu, Ag, Hg2+, Pt, Au
- Металл эместер H2, C, O2, Cl2, Br2, I2, N2, P, Si, S

Оксиддер
Туз пайда кылбоочу H2O, CO, SiO, NO, N2O
Негиздик K2O, Na2O, BaO, CaO, MgO, FeO, CrO, MnO, VO, PbO, SnO, CuO
Амфотердүү Al2O3, ZnO, Fe2O3, Cr2O3, MnO2, V2O3, PbO2, SnO2
Кислоталык Cl2O7, SO3, N2O5, P2O5, SO2↑, N2O3, P2O3, CO2↑, SiO2↓, CrO3, Mn2O7, V2O5


Негиздер
- Негиздер – металлдын атомдорунан жана алар менен байланышкан бир же бир нече гидроксил топторунан турган татаал заттар. Негиздер сууда эрүүчү жана эрибɵɵчү болуп бɵлүнɵт. Эрүүчү негиздер – щелочтор деп аталат.
- Эрүүчү негиздерге – щелочторго, валенттүүлүгү I барабар болгон металлдар, ошондой эле барий, стронций жана кальций гидроксиддери кирет.

Негиздер
- Щелочтор CsOH, RbOH, KOH, NaOH, LiOH
- Негиздер Ba(OH)2, Ca(OH)2, Mg(OH)2↓, Cu(OH)2↓, Fe(OH)2↓, Cr(OH)2↓, NH4OH начар негиздер
- Амфотердүү негиздер Al(OH)3, Zn(OH)2, Fe(OH)3, Cr(OH)3, Pb(OH)4, Sn(OH)4
![Амфотердик негиздер Негиздердин ичинен кош касиетке ээ болгон, амфотердүү негиздерди белгилеп кетели., Курамында III, IV валенттүү металлдар болгон негиздер жана цинк гидроксиди амфотердүү негиздерге кирет. Бардык амфотердик негиздер сууда эрибейт. Бир эле амфотердик негиздин формуласы ар түрдүү болушу мүмкүн. Мисалы, Al(OH)3 жана H3ALO3. Химиялык реакцияларда зат чɵйрɵгɵ карата ɵзгɵрɵт. Эгер алюминий гидроксиди кислота менен реакцияга кирсе, формуласы – Al(OH)3, ал эми щелочтор менен реакцияга киргенде, формуласы: H3ALO3 ортоалюминий кислотасы деп белгиленет. Бардык амфотердик негиздер щелочтор менен реакцияга киргенде, суу бɵлүнүп чыгат, [Zn(OH)2] башкасы), HAlO2 (метаалюминий кислотасы) да бɵлүнүп чыгыш мүмкүн.](https://fsd.multiurok.ru/html/2023/04/23/s_64455471b4f98/img6.jpg)
Амфотердик негиздер
- Негиздердин ичинен кош касиетке ээ болгон, амфотердүү негиздерди белгилеп кетели., Курамында III, IV валенттүү металлдар болгон негиздер жана цинк гидроксиди амфотердүү негиздерге кирет. Бардык амфотердик негиздер сууда эрибейт.
- Бир эле амфотердик негиздин формуласы ар түрдүү болушу мүмкүн. Мисалы, Al(OH)3 жана H3ALO3. Химиялык реакцияларда зат чɵйрɵгɵ карата ɵзгɵрɵт. Эгер алюминий гидроксиди кислота менен реакцияга кирсе, формуласы – Al(OH)3, ал эми щелочтор менен реакцияга киргенде, формуласы: H3ALO3 ортоалюминий кислотасы деп белгиленет.
- Бардык амфотердик негиздер щелочтор менен реакцияга киргенде, суу бɵлүнүп чыгат, [Zn(OH)2] башкасы), HAlO2 (метаалюминий кислотасы) да бɵлүнүп чыгыш мүмкүн.

Кислоталар
- Кислоталар деп, металлдын атомдору менен орун алмашууга жɵндɵмдүү болгон суутектин атомдорунан жана кислота калдыктарынан турган татаал заттар аталат.
- Кислотанын негиздүүлүгү анын курамындагы суутектин атомунун санына жараша болот. Негиздүүлүгүнɵ карата кислоталар бир негиздүү, эки негиздүү жана кɵп негиздүү болуп бɵлүнɵт. Мындан сырткары кислоталар кычкылтексиз (HI, HBr, HCl, HF, H 2 S↑, HCN) жана кычкылтектүү (HClO 4 , H 2 SO 4 , HNO 3 , H 4 P 2 O 7 , H 2 SO 3 ↑, H 3 PO 4 , HNO 2 , H 2 CO 3 ↑) болуп да бɵлүнɵ т.
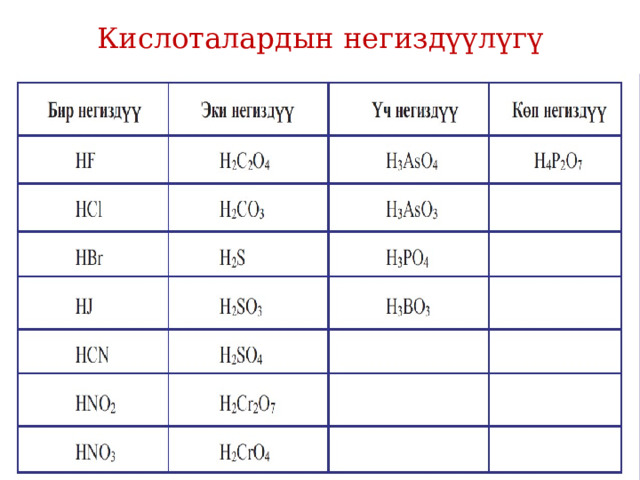
Кислоталардын негиздүүлүгү

Металлдардын активдүүлүк катары
Металлдардын ар түрдүү кислоталар менен аракеттенүүсү
![Туздар Туздар – металлдардын атомунан жана кислота калдыктарынан турган татаал заттар. Туздар орто (нормалдуу), кычкыл, негиздик, комплекстүү жана аралаш болуп бɵлүнɵт. Орто туздар Na2SO4, K2CO3↑, Ba(NO3)2, CaCO3↑, MgBr2, Na3PO4, CuSO3↑, ZnCO3↑, Al2(SO4)3 Кычкыл туздар NaHSO4, KHCO3↑, Ba(HS)2, Ca(HCO3)2↑, MgHPO4, NaH2PO4, NaHPO4, Cu(HSO3)2↑, Zn(HCO3)2↑ Негиздик туздар Ba(OH)NO3, Mg(OH)Cl, Ca(OH)I, Fe(OH)Cl2 Fe(OH)2Cl Al(OH)SO4 Zn(OH)Cl Кош туздар KNaSO4, KAl(SO4)2, NH4Fe(SO4)2 Комплекстик туздар K3[Fe(CN)6], K4[Fe(CN)6] ,[Cu(NH3)4]SO4 Аралаш туздар KClOCl](https://fsd.multiurok.ru/html/2023/04/23/s_64455471b4f98/img10.jpg)
Туздар
- Туздар – металлдардын атомунан жана кислота калдыктарынан турган татаал заттар.
- Туздар орто (нормалдуу), кычкыл, негиздик, комплекстүү жана аралаш болуп бɵлүнɵт.
- Орто туздар Na2SO4, K2CO3↑, Ba(NO3)2, CaCO3↑, MgBr2, Na3PO4, CuSO3↑, ZnCO3↑, Al2(SO4)3
- Кычкыл туздар NaHSO4, KHCO3↑, Ba(HS)2, Ca(HCO3)2↑, MgHPO4, NaH2PO4, NaHPO4, Cu(HSO3)2↑, Zn(HCO3)2↑
- Негиздик туздар Ba(OH)NO3, Mg(OH)Cl, Ca(OH)I, Fe(OH)Cl2 Fe(OH)2Cl Al(OH)SO4 Zn(OH)Cl
- Кош туздар KNaSO4, KAl(SO4)2, NH4Fe(SO4)2
- Комплекстик туздар K3[Fe(CN)6], K4[Fe(CN)6] ,[Cu(NH3)4]SO4
- Аралаш туздар KClOCl

Туздардын классификациясы
- Орто же нормалдуу туздар – суутектин атомдору металлдын атомдору менен толук орун алмашкан жана гидроксил топтору кислота калдыктары менен орун алмашкан туздар.
- Кычкыл туздар – суутектин атому металлдын атомдору менен толук орун алмашпаган туздар.
- Негиздик туздар – курамында кислоталык оксиддер менен катар гидроксил тобу болгон туздар.
- Кош туздар – суутектин атомдору эки башка металлдын атомдору менен орун алмашкан туздар.
- Комплекстик туздар – металлдын борбордук атомунан–комплекс түзүүчүдɵн жана аны курчаган лигандалардан – карама–каршы багытталган иондордон турат. Ал комплекстик туздун ички катмарынан жана ага карама–каршы багытталган сырткы катмардан турат.
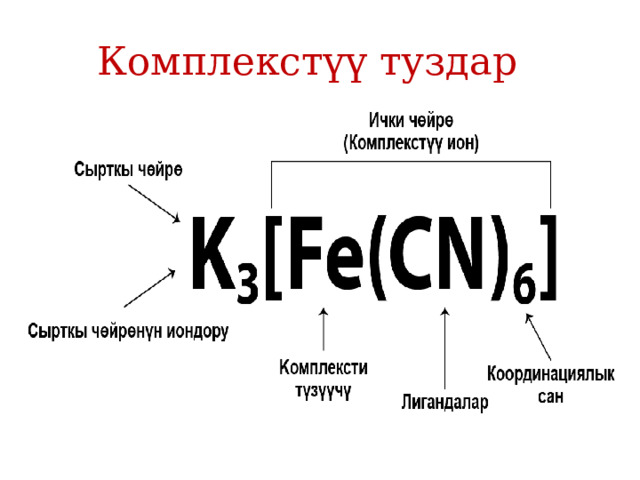
Комплекстүү туздар
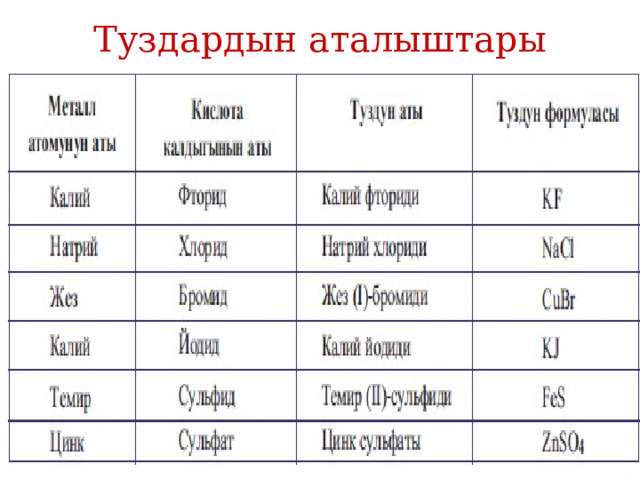
Туздардын аталыштары
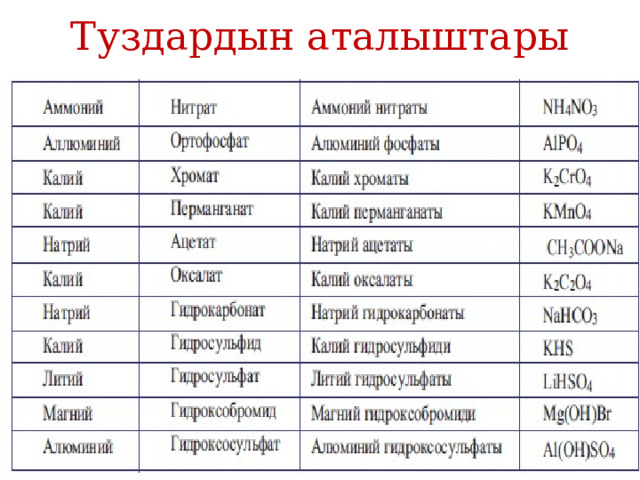
Туздардын аталыштары













![Амфотердик негиздер Негиздердин ичинен кош касиетке ээ болгон, амфотердүү негиздерди белгилеп кетели., Курамында III, IV валенттүү металлдар болгон негиздер жана цинк гидроксиди амфотердүү негиздерге кирет. Бардык амфотердик негиздер сууда эрибейт. Бир эле амфотердик негиздин формуласы ар түрдүү болушу мүмкүн. Мисалы, Al(OH)3 жана H3ALO3. Химиялык реакцияларда зат чɵйрɵгɵ карата ɵзгɵрɵт. Эгер алюминий гидроксиди кислота менен реакцияга кирсе, формуласы – Al(OH)3, ал эми щелочтор менен реакцияга киргенде, формуласы: H3ALO3 ортоалюминий кислотасы деп белгиленет. Бардык амфотердик негиздер щелочтор менен реакцияга киргенде, суу бɵлүнүп чыгат, [Zn(OH)2] башкасы), HAlO2 (метаалюминий кислотасы) да бɵлүнүп чыгыш мүмкүн.](https://fsd.multiurok.ru/html/2023/04/23/s_64455471b4f98/img6.jpg)



![Туздар Туздар – металлдардын атомунан жана кислота калдыктарынан турган татаал заттар. Туздар орто (нормалдуу), кычкыл, негиздик, комплекстүү жана аралаш болуп бɵлүнɵт. Орто туздар Na2SO4, K2CO3↑, Ba(NO3)2, CaCO3↑, MgBr2, Na3PO4, CuSO3↑, ZnCO3↑, Al2(SO4)3 Кычкыл туздар NaHSO4, KHCO3↑, Ba(HS)2, Ca(HCO3)2↑, MgHPO4, NaH2PO4, NaHPO4, Cu(HSO3)2↑, Zn(HCO3)2↑ Негиздик туздар Ba(OH)NO3, Mg(OH)Cl, Ca(OH)I, Fe(OH)Cl2 Fe(OH)2Cl Al(OH)SO4 Zn(OH)Cl Кош туздар KNaSO4, KAl(SO4)2, NH4Fe(SO4)2 Комплекстик туздар K3[Fe(CN)6], K4[Fe(CN)6] ,[Cu(NH3)4]SO4 Аралаш туздар KClOCl](https://fsd.multiurok.ru/html/2023/04/23/s_64455471b4f98/img10.jpg)






















