
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ В ОРГАНИЧЕСКОЙ ХИМИИ
«Думать легко, действовать трудно, а превратить мысль в действие — самая трудная вещь на свете» И. Гете
Окислительно-восстановительные реакции в органической химии представляют наибольший интерес, т.к. селективность перехода из одной степени окисления в другую сильно зависит от правильного выбора реагента и условий проведения реакций.
Но ОВР изучают в обязательном курсе химии недостаточно полно. Следует обратить особое внимание учащихся на окислительно-восстановительные процессы, происходящие с участием органических веществ. Это связано с тем, что окислительно-восстановительные реакции в контрольно-измерительных материалах ЕГЭ встречаются не только в заданиях С1 и С2 , но и заданиях СЗ, представляющих цепочку превращений органических веществ.
В школьных учебниках часто окислитель записывают над стрелкой как [О]. Требованием к выполнению таких заданий на ЕГЭ является обязательное обозначение всех исходных веществ и продуктов реакции с расстановкой необходимых коэффициентов. Окислительно-восстановительные реакции традиционно важны, и в то же время изучение в 10 классе, в курсе «Органическая химия» вызывает у учащихся определенные трудности.

С3 . Задания этого блока проверяют знания по органической химии
В цепочках превращений органических веществ в подавляющем большинстве заданий встречаются ОВР. Эксперт имеет право начислить балл только в том случае, если записано уравнение, а не схема реакции, т.е. верно расставлены коэффициенты. В реакциях с участием неорганических окислителей (перманганат калия, соединения хрома ( VI ), пероксид водорода и др.) сделать это бывает непросто, без электронного баланса.

Определение степени окисления атомов в молекулах органических соединений
ПРАВИЛО:
СО (атома) = число связей с более ЭО атомами минус число связей с менее ЭО атомами.
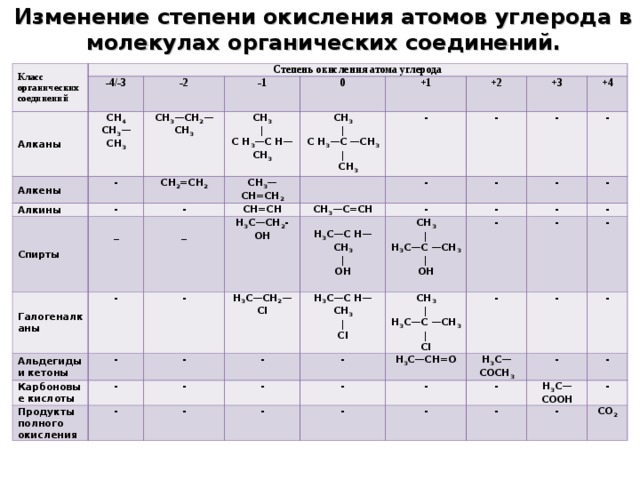
Изменение степени окисления атомов углерода в молекулах органических соединений.
Класс органических соединений
Степень окисления атома углерода
Алканы
-4/-3
CH 4
CH 3 —CH 3
Алкены
-2
Алкины
-1
CH 3 —CH 2 —CH 3
-
-
0
CH 3 | C H 3 —C H—CH 3
CH 2 =CH 2
Спирты
+1
CH 3 —CH=CH 2
-
Галогеналканы
CH 3 | C H 3 —C —CH 3 | CH 3
_
CH=CH
-
+2
Альдегиды и кетоны
_
-
-
CH 3 —C=CH
-
-
Карбоновые кислоты
-
+3
H 3 C—CH 2 - ОН
H 3 C—CH 2 — CI
-
-
Продукты полного окисления
H 3 C—C H—CH 3 |
OH
-
-
+4
-
-
-
-
-
CH 3 | H 3 C — C — CH 3 | OH
-
-
H 3 C — C H — CH 3 |
CI
-
-
-
CH 3 | H 3 C — C — CH 3 | CI
-
-
-
H 3 C—CH =O
-
-
-
-
-
H 3 C—C OCH 3
-
-
-
-
-
-
-
-
H 3 C—C OOH
-
-
-
-
CO 2


Склонность органических соединений к окислению связывают с наличием:
- кратных связей (легко окисляются алкены, алкины, алкадиены);
- функциональных групп , способных легко окисляться ( –OH, - СНО, - NH 2 );
- активированных алкильных групп , расположенных по соседству с кратными связями или бензольным кольцом (например, пропен может быть окислен до непредельного альдегида акролеина, окисление толуола до бензойной кислоты перманганатом калия в кислой среде);
- наличие атомов водорода при атоме углерода, содержащем функциональную группу .

1.МЯГКОЕ ОКИСЛЕНИЕ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Для мягкого окисления органических соединений (спиртов, альдегдов, непредельных соединений) используются соединения хрома ( VI ) – оксид хрома ( VI ), CrO 3 , дихромат калия К 2 С r 2 O 7 и др. Как правило, окисление проводится в кислой среде, продуктами восстановления являются соли хрома ( III ), например:
3CH 3 –CHO + K 2 Cr 2 O 7 + 4H 2 SO 4 → 3CH 3 –COOH + 4K 2 SO 4 + Cr 2 (SO 4 ) 3 + 4H 2 O
t
3CH 3 –CH 2 OH+2K 2 Cr 2 O 7 +8H 2 SO 4 →3CH 3 –COOH + 2K 2 SO 4 + 2Cr 2 (SO 4 ) 3 + 11H 2 O
При окислении спиртов дихроматом калия на холоду окисление можно остановить на стадии образования альдегида, при нагревании же образуются карбоновые кислоты:
3CH 3 –CH 2 OH+K 2 Cr 2 O 7 +4H 2 SO 4 →3CH 3 –C Н O+K 2 SO 4 +Cr 2 (SO 4 ) 3 +7H 2 O
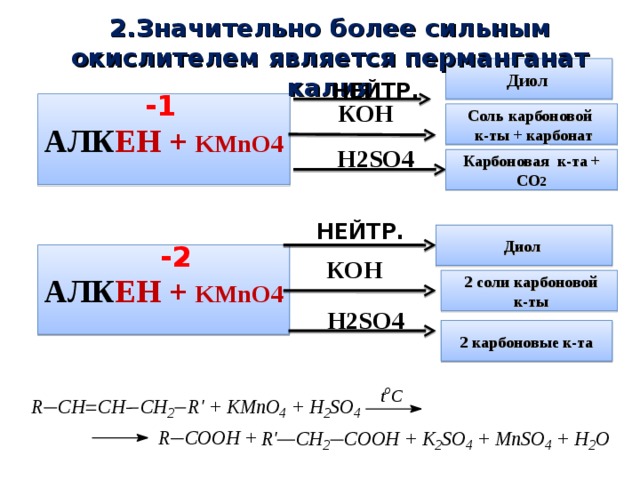
2.Значительно более сильным окислителем является перманганат калия
Диол
НЕЙТР.
-1
АЛК ЕН + KMnO4
КОН
Соль карбоновой
к-ты + карбонат
Н 2SO4
Карбоновая к-та + СО 2
НЕЙТР.
Диол
-2
АЛК ЕН + KMnO4
КОН
2 соли карбоновой
к-ты
Н 2SO4
2 карбоновые к-та
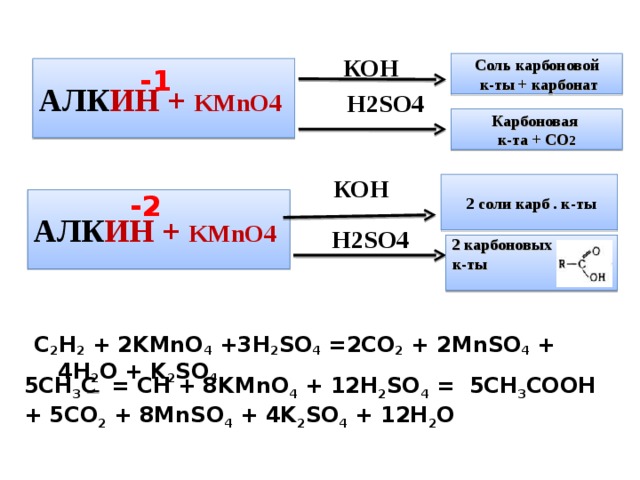
C 2 H 2 + 2KMnO 4 +3H 2 SO 4 =2CO 2 + 2MnSO 4 + 4H 2 O + K 2 SO 4
КОН
Соль карбоновой
к-ты + карбонат
-1
АЛК ИН + KMnO4
Н 2SO4
Карбоновая
к-та + СО 2
КОН
2 соли карб . к-ты
-2
АЛК ИН + KMnO4
Н 2SO4
2 карбоновых
к-ты
5CH 3 C = CH + 8KMnO 4 + 12H 2 SO 4 = 5CH 3 COOH + 5CO 2 + 8MnSO 4 + 4K 2 SO 4 + 12H 2 O
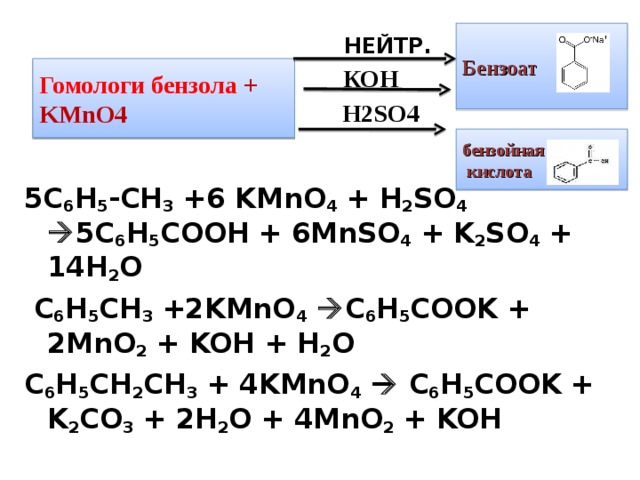
5C 6 H 5 -CH 3 +6 KMnO 4 + H 2 SO 4 5C 6 H 5 COOH + 6MnSO 4 + K 2 SO 4 + 14H 2 O
C 6 H 5 CH 3 +2KMnO 4 C 6 H 5 COOK + 2MnO 2 + KOH + H 2 O
C 6 H 5 CH 2 CH 3 + 4KMnO 4 C 6 H 5 COOK + K 2 CO 3 + 2H 2 O + 4MnO 2 + KOH
Бензоат
НЕЙТР.
Гомологи бензола + KMnO4
КОН
Н 2SO4
бензойная
кислота

Окислительно-восстановительные свойства кислородсодержащих соединений
Окислителями спиртов чаще всего являются оксид меди ( II ) или
перманганат калия, а окислителями альдегидов и кетонов - гидроксид меди ( II ), аммиачный раствор оксида серебра и другие
окислители
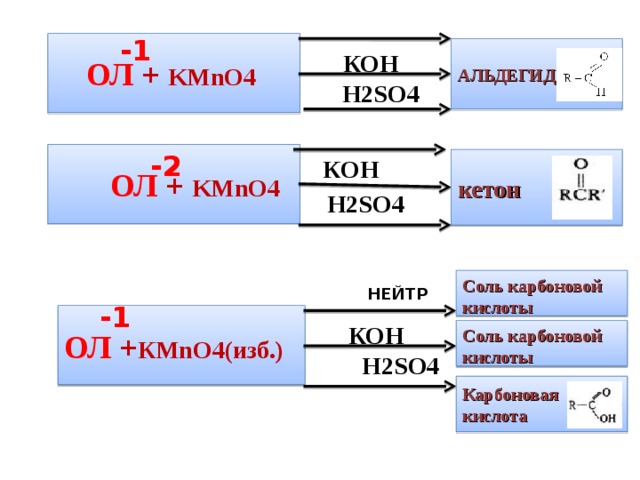
-1
ОЛ + KMnO4
АЛЬДЕГИД
КОН
Н 2SO4
-2
ОЛ + KMnO4
кетон
КОН
Н 2SO4
Соль карбоновой кислоты
НЕЙТР
-1
ОЛ + К MnO4 (изб.)
КОН
Соль карбоновой кислоты
Н 2SO4
Карбоновая кислота
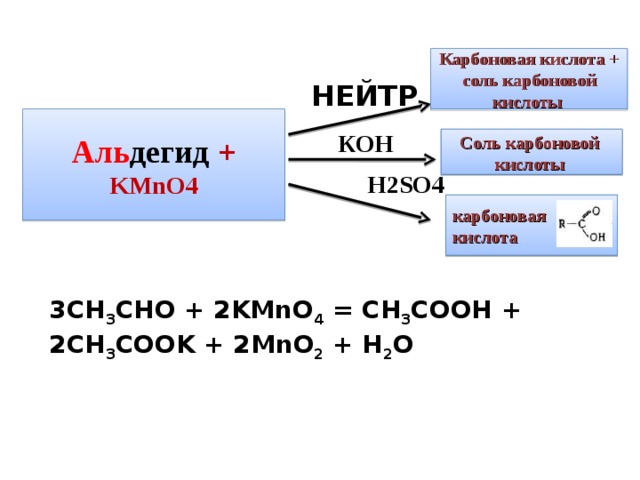
Карбоновая кислота +
соль карбоновой кислоты
НЕЙТР .
Аль дегид + KMnO4
КОН
Соль карбоновой
кислоты
Н 2SO4
карбоновая
кислота
3CH 3 CHO + 2KMnO 4 = CH 3 COOH + 2CH 3 COOK + 2MnO 2 + H 2 O
![Альдегиды – довольно сильные восстановители, и поэтому легко окисляются различными окислителями CH 3 CHO + 2[Ag(NH 3 ) 2 ]OH CH 3 COONH 4 + 2Ag + H 2 O + 3NH 3](https://fsd.multiurok.ru/html/2018/01/23/s_5a671b17bdb40/img14.jpg)
Альдегиды – довольно сильные восстановители, и поэтому легко окисляются различными окислителями
CH 3 CHO + 2[Ag(NH 3 ) 2 ]OH CH 3 COONH 4 + 2Ag + H 2 O + 3NH 3
Алгоритм подбора коэффициентов
Поскольку в задании С3 при составлении уравнений ОВР не требуется написания уравнений электронного баланса, подбирать коэффициенты удобно методом подстрочного баланса – упрощенным способом баланса электронного.
1 . Составляется схема ОВР. Например, для окисления толуола до бензойной кислоты подкисленным раствором перманганата калия схема реакции такова:
С 6 Н 5 -СН 3 + KMnO 4 + H 2 SO 4 С 6 Н 5 -С OO Н + K 2 SO 4 + MnSO 4 + H 2 O
2. Указываются с.о. атомов. С.о. атома углерода определяется по приведенному выше способу.
С 6 Н 5 -С -3 Н 3 + KMn +7 O 4 + H 2 SO 4 С 6 Н 5 -С +3 OO Н + K 2 SO 4 + Mn +2 SO 4 + H 2 O
3. Число электронов, отданных атомом углерода (6), записывается как коэффициент перед формулой окислителя (перманганата калия):
С 6 Н 5 -С -3 Н 3 + 6 KMn +7 O 4 + H 2 SO 4 С 6 Н 5 -С +3 OO Н + K 2 SO 4 + Mn +2 SO 4 + H 2 O
4. Число электронов, принятых атомом марганца (5), записывается как коэффициент перед формулой восстановителя (толуола):
5 С 6 Н 5 -С -3 Н 3 + 6 KMn +7 O 4 + H 2 SO 4 С 6 Н 5 -С +3 OO Н + K 2 SO 4 + Mn +2 SO 4 + H 2 O
5. Важнейшие коэффициенты на месте. Дальнейший подбор не составляет труда:
5 С 6 Н 5 -СН 3 + 6 KMnO 4 + 9 H 2 SO 4 5 С 6 Н 5 -С OO Н + 3 K 2 SO 4 + 6 MnSO 4 + 14 H 2 O
Пример тестового задания(С3)
1. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Hg 2+ , H + KMnO 4 , H + С l 2 (эквимол.), h
С 2 Н 2 Х 1 СН 3 СООН Х 2 СН 4 X 3
1. реакция Кучерова.
Hg 2+ , H +
CH CH + H 2 O CH 3 CHO
2.Альдегиды легко окисляются до карбоновых кислот, в том числе таким сильным окислителем, как перманганат калия в кислой среде.
CH 3 CHO + KMnO 4 + H 2 SO 4 CH 3 COOH + K 2 SO 4 + MnSO 4 + H 2 O
СН 3 С +1 Н О + KMn +7 O 4 + H 2 SO 4 СН 3 -С +3 OO Н + K 2 SO 4 + Mn +2 SO 4 + H 2 O
5 CH 3 CHO + 2 KMnO 4 + 3 H 2 SO 4 5 CH 3 COOH + K 2 SO 4 + 2 MnSO 4 + 3 H 2 O
3.Для выполнения следующего звена цепочки необходимо оценить вещество Х 2 с двух позиций: во-первых, оно в одну стадию образуется из уксусной кислоты, во-вторых, из него можно получить метан. Это вещество – ацетат щелочного металла. Записываются уравнения третьей и четвертой реакций.
CH 3 COOH + NaOH CH 3 COONa + H 2 O
сплавление
4. CH 3 COONa + NaOH CH 4 + Na 2 CO 3
5.Условия протекания следующей реакции (свет) однозначно указывают на ее радикальный характер. С учетом указанного соотношения реагентов (эквимолярное) записывается уравнение последней реакции:
h
CH 4 + Cl 2 CH 3 Cl + HCl

Сайты тренажеры:
- http://reshuege.ru/ (Решу ЕГЭ)
- http://4ege.ru/himiya/4181-demoversiya-ege-po-himii-2014.html (ЕГЭ портал)
- http://www.alleng.ru/edu/chem3.htm (Образовательные ресурсы Интернета - Химия)
- http://ege.yandex.ru/ (онлайн-тесты)




















![Альдегиды – довольно сильные восстановители, и поэтому легко окисляются различными окислителями CH 3 CHO + 2[Ag(NH 3 ) 2 ]OH CH 3 COONH 4 + 2Ag + H 2 O + 3NH 3](https://fsd.multiurok.ru/html/2018/01/23/s_5a671b17bdb40/img14.jpg)





















