Мкт и уравнение состояния
Так как молярная масса атомарного кислорода равна 16 г/моль, а атома гелия – 4г/моль, то масса молекулы кислорода больше массы атома гелия:
1) в 4 раза; 2) в 2 раза; 3) в 8 раз 4) в 16 раз
2. Если 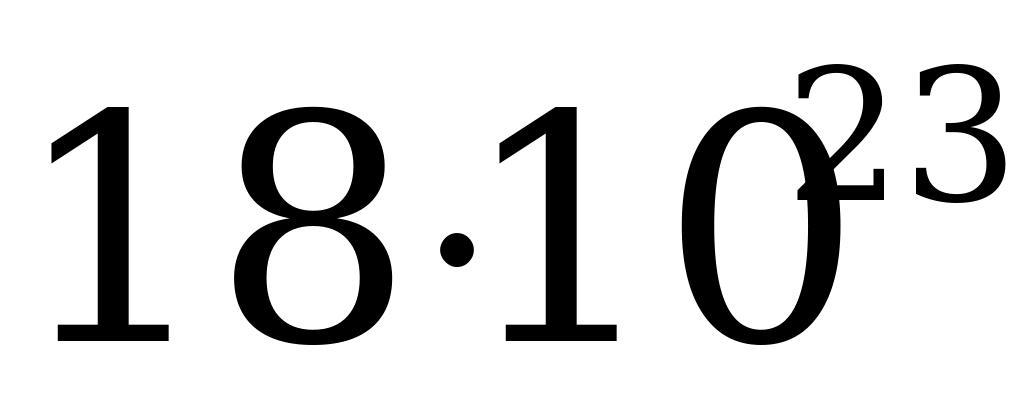 молекул углекислого газа нагреть до определенной температуры, при которой молекулы полностью распадаются, то в сосуде будет количество вещества приблизительно равное:
молекул углекислого газа нагреть до определенной температуры, при которой молекулы полностью распадаются, то в сосуде будет количество вещества приблизительно равное:
1) 6 моль; 2) 18 моль; 3) 54 моль; 4) 12 моль;
3. Молярная масса смеси двух газов находится по формуле:
1) 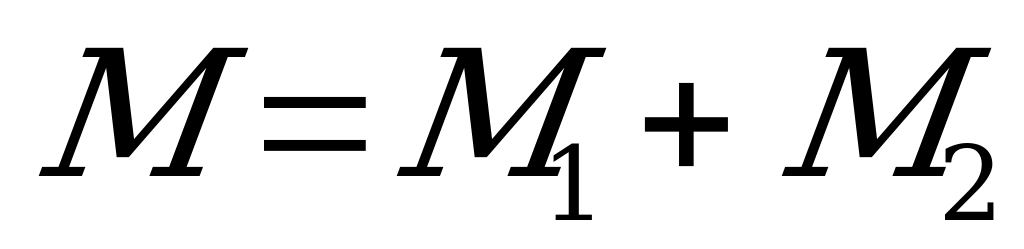 2)
2)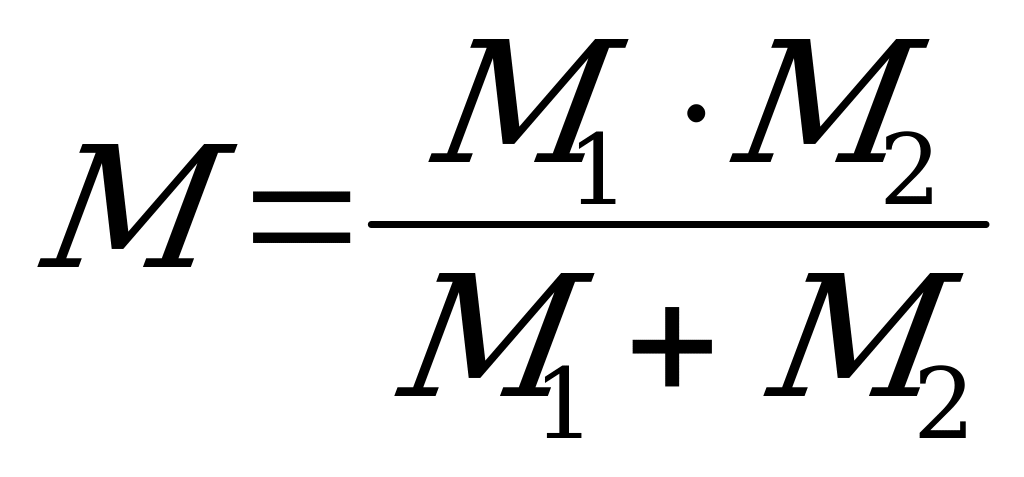 3)
3)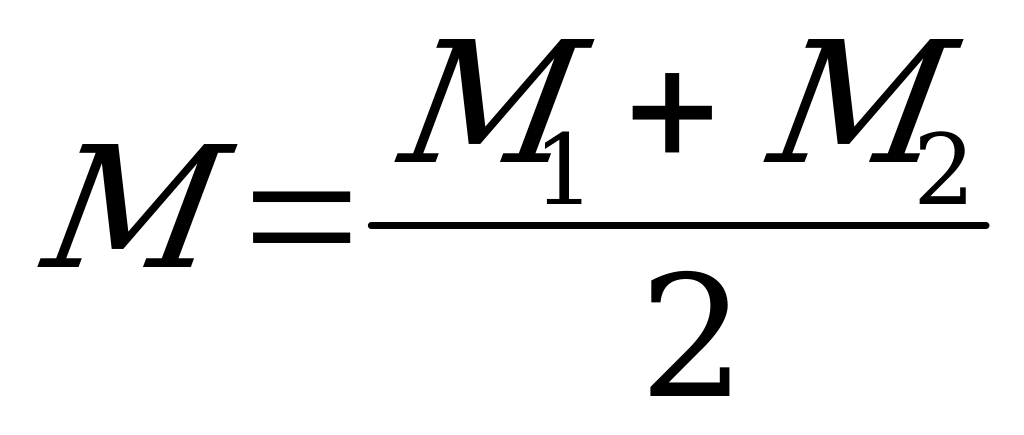 4)
4)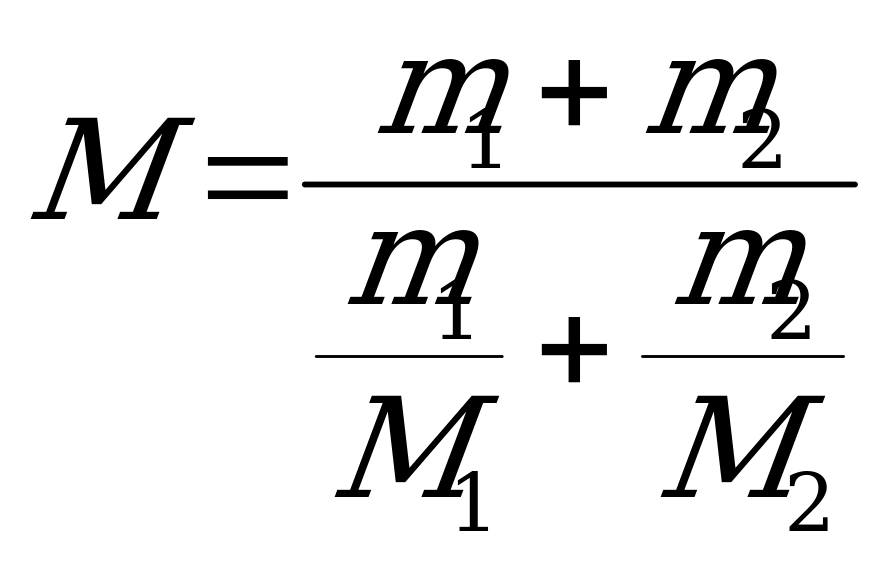
4. Если два газа долгое время находятся в одном сосуде, то справедливым не является утверждение:
1) равны средние квадратические скорости; 2) равны абсолютные температуры;
2) равны средние кинетические энергии; 4) равны давления газов;
5. Изменение температуры на 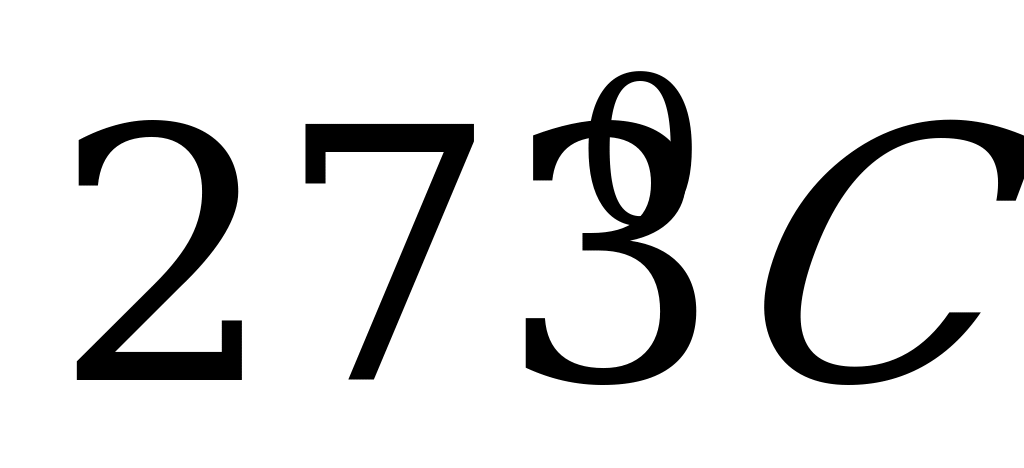 соответствует изменению температуры в (
соответствует изменению температуры в (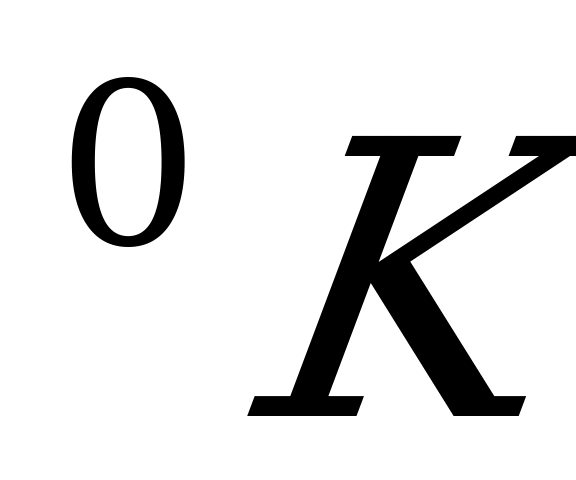 ) на:
) на:
1) 0 2) 546 3) 273 4) нет верного
6. Универсальная газовая постоянная находится из соотношения R=:
1) 
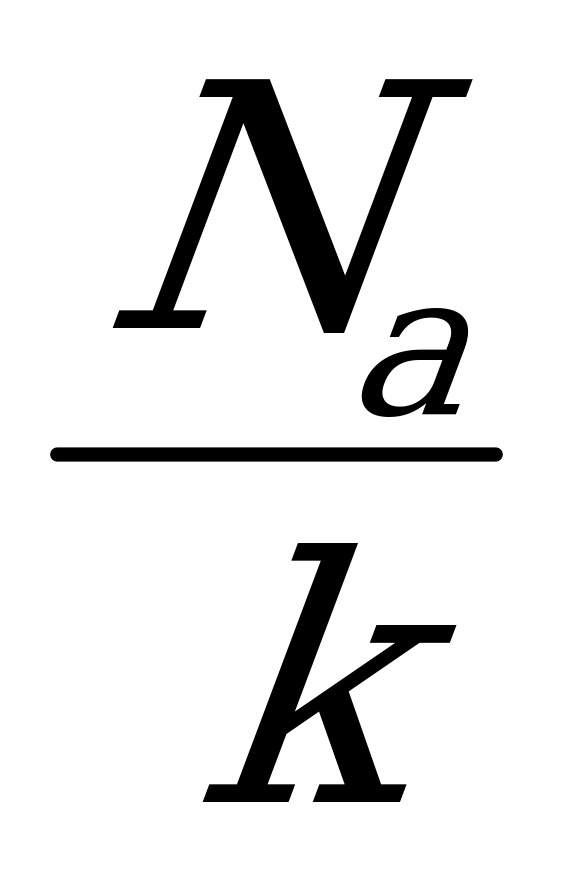 2)
2) 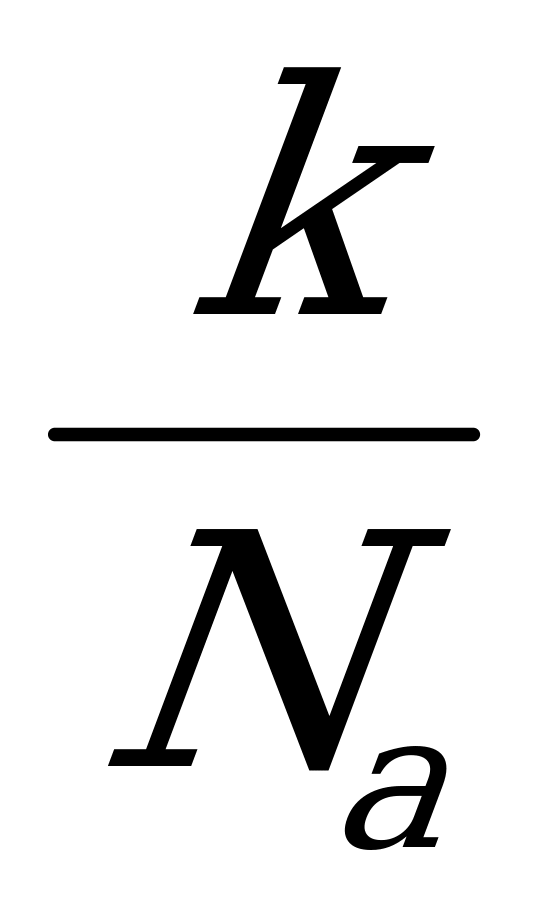 3)
3) 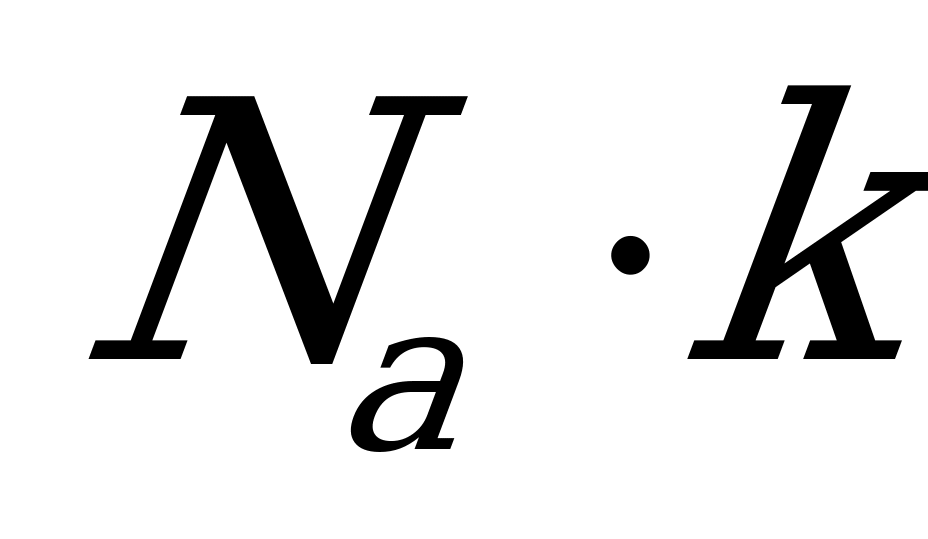 4) нет верного
4) нет верного
7. Давление смеси газов:
1) больше давления каждого газа; 2) меньше давления каждого;
3) равно среднему арифметическому; 4) равно разности большего и меньшего парциального;
8. В вертикальном цилиндре под поршнем находится идеальный газ. Условие равновесия поршня через равенство давлений можно применить, если:
1) верхняя и нижняя поверхности поршня – горизонтальные плоскости;
2) только верхняя поверхность – горизонтальная плоскость;
3) только нижняя поверхность – горизонтальная плоскость;
4) форма поверхности не имеет значения;
9. Исходя из физического смысла абсолютной температуры, если газ в закрытом сосуде нагревают, то это приводит к:
1) увеличению средней кинетической энергии движения частиц;
2) увеличению средней квадратической скорости;
3) уменьшению энергии взаимодействия молекул;
4) увеличению хаоса в сосуде;
10. Если названия изопроцессов пометить цифрами: 1 – изотермический; 2 – изобарный; 3 – изохорный; а математические выражения буквами: а – 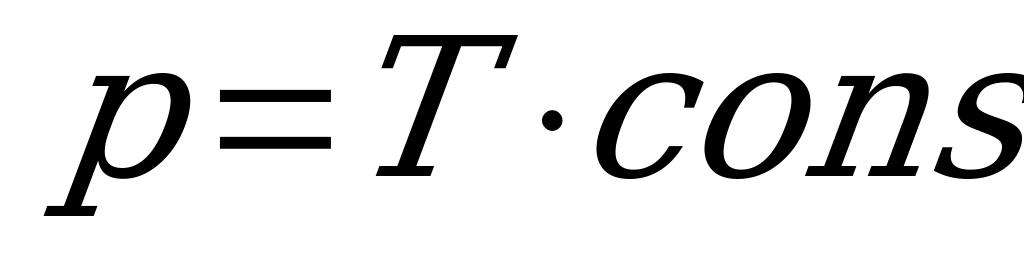 ; в -
; в - 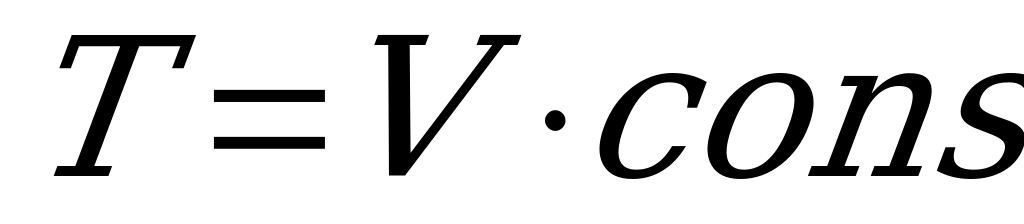 ; с -
; с - 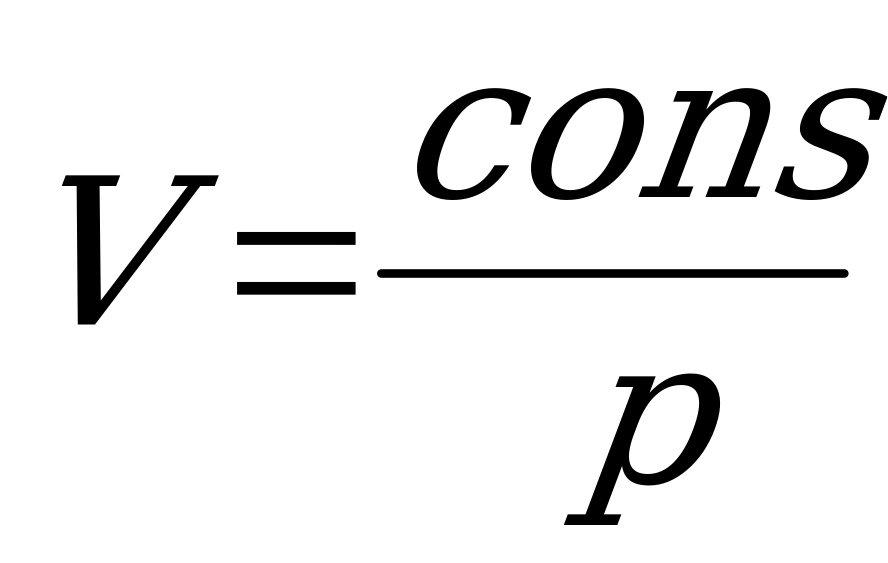 , то не правильное соответствие имеет вид:
, то не правильное соответствие имеет вид:
1) 1 – с; 2) 2 – в; 3) 3 – а; 4) 2 – а;
11. Для данного графика некоторого процесса если двигаться от точки 1 к точке 2 то возможно не верным является утверждение:
1) увеличивается давление; 2) увеличивается объем; 3) увеличивается температура; 4) все верны;
12. Нормальными называются условия:
1) 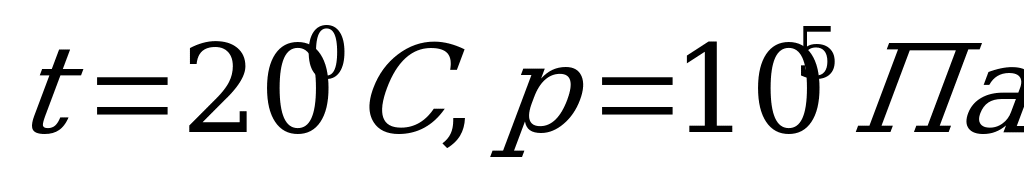 2)
2)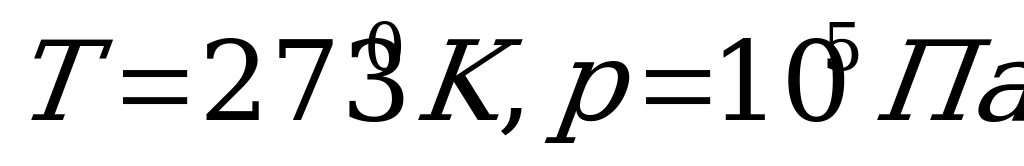 3)
3)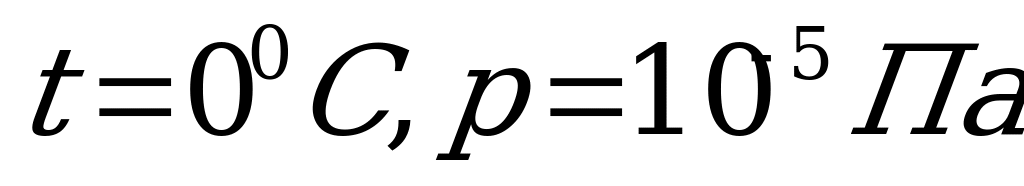 4) нет верного
4) нет верного
13. Давление идеального газа на стенки сосуда с точки зрения МКТ обусловлено:
1) только упругими ударами молекул; 2) только неупругими ударами;
3) любыми ударами; 4) только ударами перпендикулярно стенке
14. Плотность смеси двух газов в замкнутом сосуде находят по формуле:
1)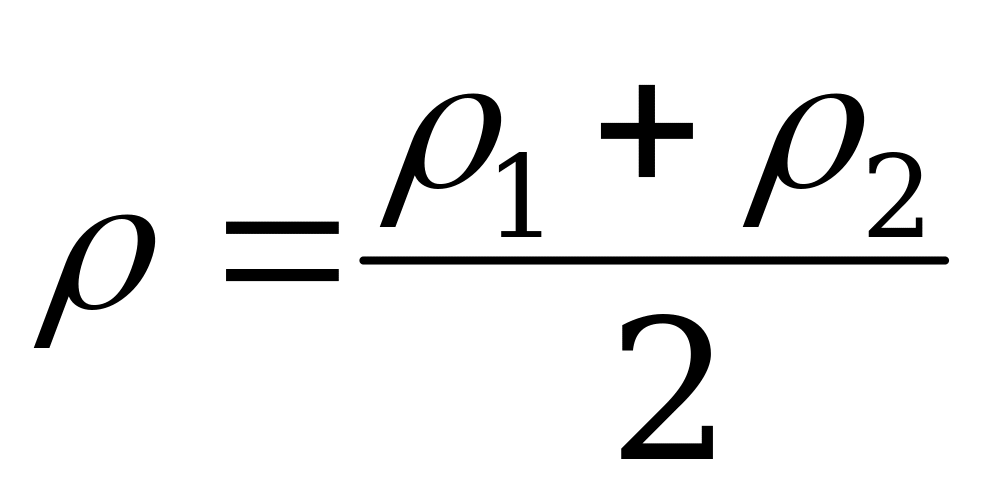 ; 2)
; 2)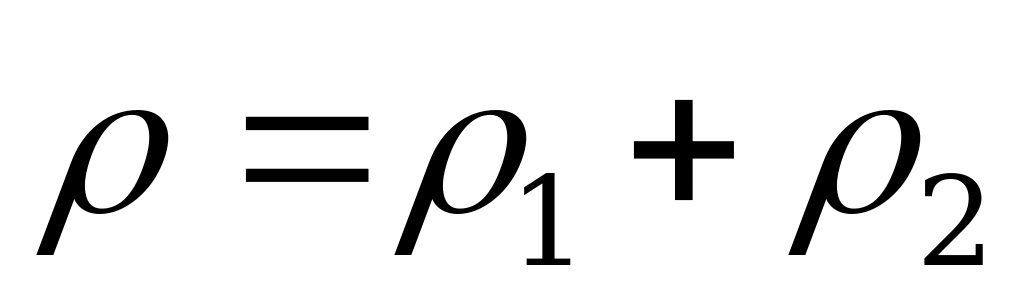 3)
3) 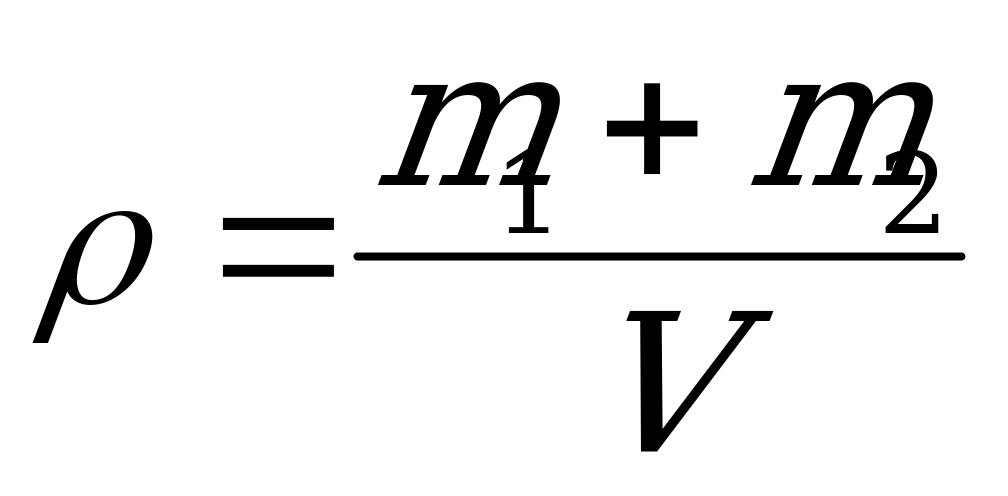 4)
4)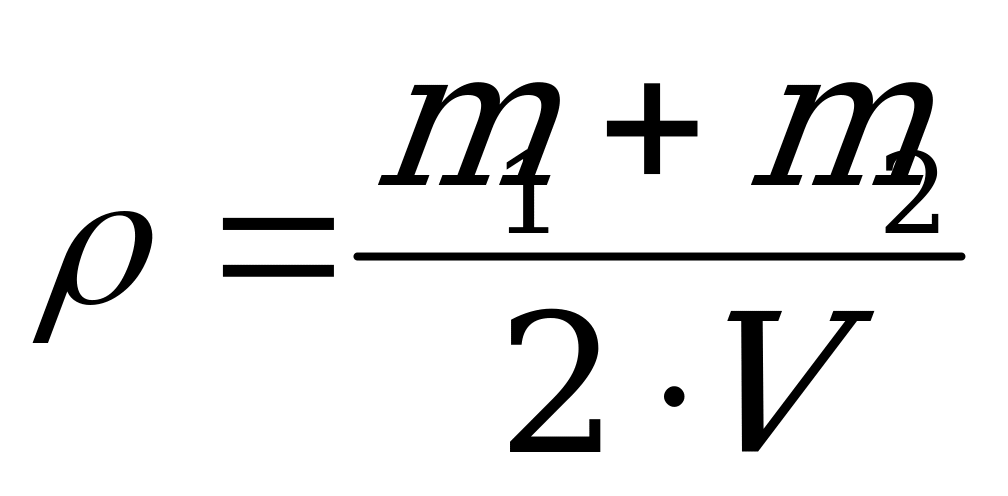
15. Если давление газа увеличить в 4 раза, а объем – в 2 раза, то температура понизится:
1) в 2 раза; 2) в 4 раза; 3) в 8 раз; 4) нет верного;
16. В изображенном на рисунке сосуде давление под закрытым правым торцом равно:
1) 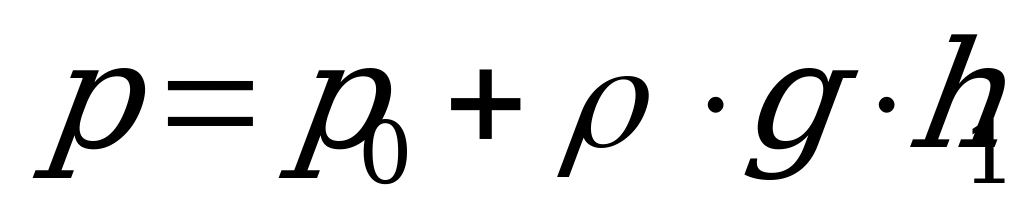 2)
2) 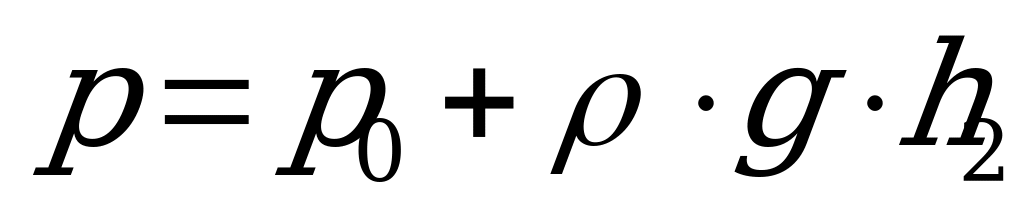 3)
3) 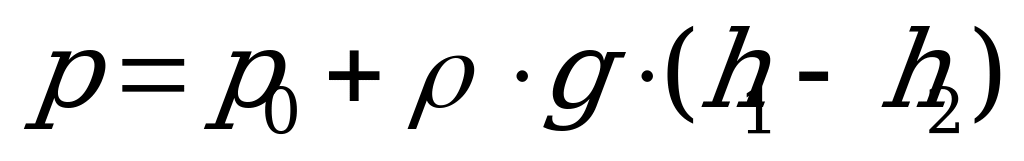 4)
4)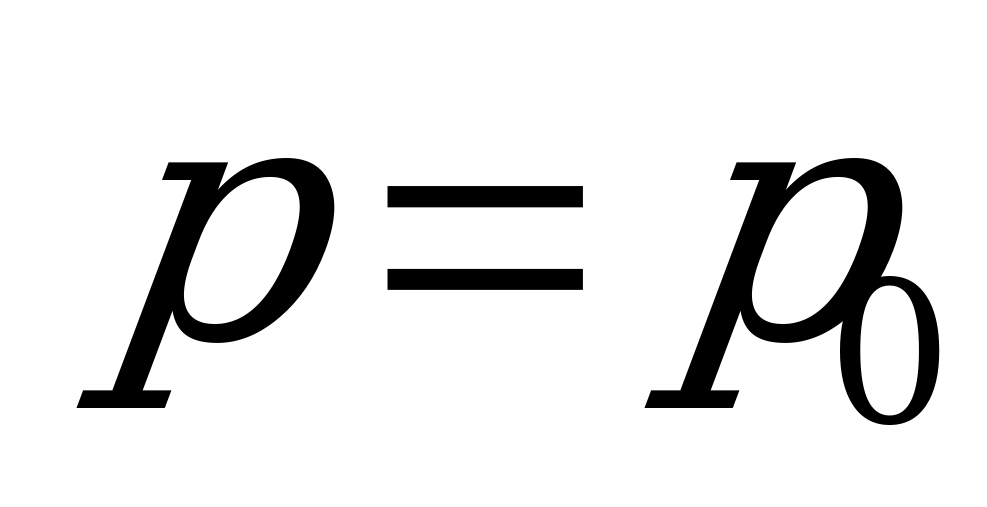
17. Если при неизменных объеме сосуда и температуре, давление газа понижается, то это не значит, что в сосуде
1) уменьшается количество частиц; 2) уменьшается среднее расстояние между частицами;
3) уменьшается количество вещества; 4) постоянна средняя квадратическая скорость частиц;
18. Манометр подключенный к сосуду вокруг которого нормальные условия показывает давление 4 атм. Действительное давление газа в сосуде равно:
1) 4 атм. 2) 3 атм. 3) 5 атм. 4) нельзя найти.
19. В трубке с закрытым нижним и открытым верхним концами под столбом ртути заперт газ. Если трубку поднимать равномерно вертикально вверх (на сотни километров), то столбик ртути будет смещаться:
1) вниз; 2) вверх; 3) остается на месте; 4) нет верного.
20. За этот тест вы получите оценку:
1) 2 балла; 2) 3 балла; 3) 4 балла; 4) 5 баллов.