62 урок Контрольная работа №4 по теме «Важнейшие р-элементы и их соединения» 10 класс 1 час
Дата: _________
Цель:
Обобщить знания и умения учащихся по теме «p-элементы» и уровень сформированности в написании строения атома, химических уравнений, физических свойств и применение р-элементов.
Формирование умений доказывать, разрешать проблемы, обобщать знания. Развитие умений владеть собой, уверенности в своих силах
Воспитать самостоятельность, трудолюбие
Тип урока: урок проверки, оценки и коррекции знаний, навыков и умений:
Форма урока: контрольная работа в виде теста
Методы обучения: письменная работа контролирующего характера
Ход урока
1. Организационный момент. Приветствие ребят. Проверка готовности к уроку. Целевая установка
2. Актуализация ЗУН
Фронтальная беседа: Какие темы были изучены и повторены нами на предыдущих уроках? (По этим темам сегодня пишете контрольную работу)
Провожу инструктаж по выполнению КР
Не разрешается пользоваться учебниками (только форзац), тетрадями
Не допускаются разговоры во время выполнения КР
Оформление работы - Работа по вариантам, вопросы теста не переписывать
Выполнять задания в любой последовательности
3. Этап контроля знаний
Выполнение теста по вариантам
1 ВАРИАНТ
Для всех галогенов характерны:
| А) высокие восстановительные свойства | Б) окислительные свойства |
| В) высокая реакционная способность | В) газообразное состояние простых веществ при обычных условиях |
Галогены реагируют с водой, водородом, кислородом, оксидом цинка, медью, фосфором, бензолом. Сколько ошибок в этом утверждении?
Среди галогенов восстановительные свойства наиболее ярко выражены у:
Атомы серы и кислорода сходны по:
| А) заряду ядра | Б) числу энергетических уровней |
| В) числу электронов на внешнем уровне | Г) числу нейтронов |
Сера проявляет следующие степени окисления:
| А) -2, -4, +6, +8 | Б) -1, 0, +2, +4 | В) -2, +6, +4, 0 | Г) -2, -4, -6, 0 |
С помощью, каких катионов можно обнаружить присутствие в водном растворе сульфид-ионы:
| А) K+ | Б) Cu2+ | В) Pb2- | Г) Na+ |
Серную кислоту и ее соли можно распознать с помощью?
| А) индикаторов | Б) растворов солей бария |
| В) реакции нейтрализации | Г) медной проволоки |
Какая схема отражает промышленный способ получения азота?
| А) воздух  | Б) NH4NO2→ | В) HNO3→ | Г) NH4NO3→ |
В какой реакции азот является восстановителем?
| А) N2 + O2→ | Б) N2 + H2→ | В) N2 + Li→ | Г) N2 + Mg→ |
Молекула аммиака имеет форму:
| А) изогнутую | Б) линейную | В) плоскую | Г) пирамидальную |
Какой металл пассивируется при реакции с концентрированной HNO3?
Белый фосфор более активен, чем азот, так как:
| А) заряд ядра атома фосфора меньше | Б) молекулы фосфора имеют большую массу |
| В) число протонов в ядре атома азота меньше, чем у фосфора | Г) энергия связи между атомами в молекуле белого фосфора меньше, чем в молекуле азота |
С какими веществами реагирует как ортофосфорная, так и азотная разбавлена кислота:
| А) серебром | Б) оксидом кальция | В) гидроксидом калия | Г) аммиаком |
В ряду C → Si → Ge → Sn → Pb неметаллические признаки элементов:
| А) усиливаются | Б) ослабевают | В) не изменяются | Г) усиливаются, а затем ослабевают |
Аллотропные видоизменения (алмаз, графит, карбин) имеют:
| А) различные физические и сходные химические свойства |
| Б) различные физические и химические свойства |
| В) сходные физические и химические свойства |
| Г) различные химические и сходные физические свойства |
Адсорбция представляет собой:
| А) обесцвечивание красителей | Б) взаимодействие угля и газов |
| В) поглощение газов поверхностью твердого вещества | Г) один из способов очистки веществ |
Углерод проявляет свойства восстановителя, реагируя с:
| А) водородом | Б) кислородом | В) алюминием | Г) оксидом меди (II) |
Найдите соответствие между химическими и техническими названиями соединений углерода:
| 1) мел | А) гидрокарбонат натрия |
| 2) поташ | Б) карбонат кальция |
| 3) кальцинированная сода | В) карбонат калия |
| 4) питьевая сода | Г) карбонат натрия |
Качественной реакцией на ион CO32- является
| А) изменение окраски индикатора | Б) выпадение белого творожистого осадка |
| В) образование желтого осадка | Г) «вскипание» раствора при действии сильной кислоты за счет выделения СО2 |
Кремниевая кислота не может образовываться в результате реакций:
| А) SiO2 + H2O → | Б) Na2SiO3 + H2O + SO2 → |
| В) K2SiO3 + H2O + CO2 → | Г) Si + H2SO4 → |
21. Масса оксида кальция, необходимая для взаимодействия с фосфорной кислотой, если получается 62 г фосфата кальция
| A) 31,8 г | B) 32,4 г | C) 43,5 г | D) 33,6 г | E) 48,4 г |
2 ВАРИАНТ
В ряду галогенов с возрастанием атомного номера:
| А) плотность простых веществ увеличивается, интенсивность окраски усиливается |
| Б) плотность уменьшается, интенсивность окраски усиливается |
| В) плотность увеличивается, интенсивность окраски ослабевает |
| Г) плотность веществ уменьшается, интенсивность окраски ослабевает |
Галогены в реакциях могут проявлять:
| А) только окислительные свойства |
| Б) только восстановительные свойства |
| В) окислительные и восстановительные свойства |
| Г) галогены не проявляют окислительно-восстановительные свойства |
Выберите правильный ответ.
Степень окисления +4 сера имеет в составе:
| А) Al2(SO4)3 | Б) Na2SO3 | В) Ca(HCO3)2 | Г) K2S |
Укажите формулы веществ, в состав которых входит сера проявляет свою максимальную степень окисления:
| А) FeS2 | Б) H2SO4 | В) SO2 | Г) SO3 |
Укажите схемы осуществимых реакций с участием сероводородной кислоты:
| А) K2S + H2S → | Б) H2S + KCl → | В) H2S + CuSO3 → | Г) KHS + H2S → |
С помощью, каких веществ можно обнаружить в растворе сульфат-ион?
| А) хлорид бария | Б) хлорид калия | В) нитрат серебра (I) | Г) нитрат натрия |
При определенных условиях концентрированная серная кислота реагирует с:
| А) железом | Б) нитратом натрия | В) ортофосфатом кальция | Г) оксидом меди (II) |
Концентрированная серная кислота, в отличие от разбавленной серной кислоты:
| А) при обычных условиях реагирует с железом и алюминием |
| Б) вытесняет из кристаллических хлоридов хлороводород |
| В) является окислителем за счет ионов H+ (Н3О+) |
| Г) является окислителем за счет ионов S6+ (SO42-) |
Азот и фосфор:
| А) находятся в одном периоде | Б) находятся в одной группе |
| В) находятся в разных подгруппах | Г) имеют одинаковое строение |
Азот в составе аммиака является:
| А) только окислителем | Б) только восстановителем |
| В) и окислителем, и восстановителем | Г) донором электронов |
Для определения нитрат-ионов необходимо взять:
| А) соль свинца | Б) соль серебра |
| В) ионы медь | Г) ионы золота |
Фосфор является восстановителем, реагируя с:
| А) магнием | Б) бертолетовой солью |
| В) хлором | Г) серой |
Чему равны валентность и степень окисления фосфора в H3PO4?
| А) III и +3 | Б) V и +3 | В) III и +5 | Г) V и +5 |
С каким веществом не реагирует H3PO4, но реагирует HNO3 разб?
| А) карбонатом калия | Б) оксидом кальция | В) медью | Г) карбонатом аммония |
Сколько аллотропных видоизменений образует углерод?
Поглощение поверхностью твердого вещества газов или растворимых веществ называется:
| А) регенерацией | Б) возгонкой | В) адсорбцией | Г) дистилляцией |
Отметьте схемы реакций, в результате которых выделяется оксид углерода (IV):
| А) Na2CO3 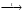 | Б) NaHCO3 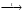 | В) CaCO3 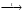 | Г) CaCO3 + HCl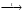 |
При обработке карбоната металла кислотой образуется:
| А) С (тв.) | Б) О2 (г) | В) СО (г) | Г) СО2 (г) |
В реакциях с азотом, углеродом и серой кремний проявляет свойства:
| А) окислителя | Б) восстановителя в реакции с азотом, окислителя в реакциях с серой и углеродом |
| В) восстановителя | Г) окислителем в реакции с углеродом, восстановителя в реакциях с азотом и серой |
Состав оконного стекла выражается формулой:
| А) Na2O·CaO·6SiO2 | Б) Mg3H4Si2O9 | В) CaAl2Si2O8 | Г) Al2O3·2SiO2·2H2O |
21. Масса серной кислоты, содержащаяся в 500 мл 0,2 М раствора
| A) 4,9 г | B) 9,8 г | C) 14,7 г | D) 19,6 г | E) 24,5 г |
Ответы Контрольная работа №4 по теме «p-элементы» 10 класс
| 1 вариант | 2 вариант |
| 1 | Б | 12 | В | 1 | А | 12 | В |
| 2 | Г | 13 | В | 2 | В | 13 | Г |
| 3 | В | 14 | Б | 3 | Б | 14 | В |
| 4 | В | 15 | А | 4 | Б | 15 | Б |
| 5 | В | 16 | В | 5 | А | 16 | В |
| 6 | В | 17 | А | 6 | А | 17 | В |
| 7 | А | 18 | 1-Б 2-В 3-Г 4-А | 7 | Б | 18 | Г |
| 8 | А | 19 | Б | 8 | А | 19 | Б |
| 9 | Г | 20 | А | 9 | Б | 20 | А |
| 10 | Г | 21 | D | 10 | Г | 21 | B |
| 11 | Б |
|
| 11 | Б |
|
|
Контрольная работа №4 по теме «p-элементы» 10 класс
1 ВАРИАНТ
1. Для всех галогенов характерны:
| А) высокие восстановительные свойства | Б) окислительные свойства |
| В) высокая реакционная способность | В) газообразное состояние простых веществ при обычных условиях |
2. Галогены реагируют с водой, водородом, кислородом, оксидом цинка, медью, фосфором, бензолом. Сколько ошибок в этом утверждении?
3. Среди галогенов восстановительные свойства наиболее ярко выражены у:
4. Атомы серы и кислорода сходны по:
| А) заряду ядра | Б) числу энергетических уровней |
| В) числу электронов на внешнем уровне | Г) числу нейтронов |
5. Сера проявляет следующие степени окисления:
| А) -2, -4, +6, +8 | Б) -1, 0, +2, +4 | В) -2, +6, +4, 0 | Г) -2, -4, -6, 0 |
6. С помощью, каких катионов можно обнаружить присутствие в водном растворе сульфид-ионы:
| А) K+ | Б) Cu2+ | В) Pb2- | Г) Na+ |
7. Серную кислоту и ее соли можно распознать с помощью?
| А) индикаторов | Б) растворов солей бария | В) реакции нейтрализации | Г) медной проволоки |
8. Какая схема отражает промышленный способ получения азота?
| А) воздух  | Б) NH4NO2→ | В) HNO3→ | Г) NH4NO3→ |
9. В какой реакции азот является восстановителем?
| А) N2 + O2→ | Б) N2 + H2→ | В) N2 + Li→ | Г) N2 + Mg→ |
10. Молекула аммиака имеет форму:
| А) изогнутую | Б) линейную | В) плоскую | Г) пирамидальную |
11. Какой металл пассивируется при реакции с концентрированной HNO3?
12. Белый фосфор более активен, чем азот, так как:
| А) заряд ядра атома фосфора меньше | Б) молекулы фосфора имеют большую массу |
| В) число протонов в ядре атома азота меньше, чем у фосфора | Г) энергия связи между атомами в молекуле белого фосфора меньше, чем в молекуле азота |
13. С какими веществами реагирует как ортофосфорная, так и азотная разбавлена кислота:
| А) серебром | Б) оксидом кальция | В) гидроксидом калия | Г) аммиаком |
14. В ряду C → Si → Ge → Sn → Pb неметаллические признаки элементов:
| А) усиливаются | Б) ослабевают | В) не изменяются | Г) усиливаются, а затем ослабевают |
15. Аллотропные видоизменения (алмаз, графит, карбин) имеют:
| А) различные физические и сходные химические свойства |
| Б) различные физические и химические свойства |
| В) сходные физические и химические свойства |
| Г) различные химические и сходные физические свойства |
16. Адсорбция представляет собой:
| А) обесцвечивание красителей | Б) взаимодействие угля и газов |
| В) поглощение газов поверхностью твердого вещества | Г) один из способов очистки веществ |
17. Углерод проявляет свойства восстановителя, реагируя с:
| А) водородом | Б) кислородом | В) алюминием | Г) оксидом меди (II) |
18. Найдите соответствие между химическими и техническими названиями соединений углерода:
| 1) мел | А) гидрокарбонат натрия |
| 2) поташ | Б) карбонат кальция |
| 3) кальцинированная сода | В) карбонат калия |
| 4) питьевая сода | Г) карбонат натрия |
19. Качественной реакцией на ион CO32- является
| А) изменение окраски индикатора | Б) выпадение белого творожистого осадка |
| В) образование желтого осадка | Г) «вскипание» раствора при действии сильной кислоты за счет выделения СО2 |
20. Кремниевая кислота не может образовываться в результате реакций:
| А) SiO2 + H2O → | Б) Na2SiO3 + H2O + SO2 → |
| В) K2SiO3 + H2O + CO2 → | Г) Si + H2SO4 → |
21. Масса оксида кальция, необходимая для взаимодействия с фосфорной кислотой, если получается 62 г фосфата кальция
| A) 31,8 г | B) 32,4 г | C) 43,5 г | D) 33,6 г | E) 48,4 г |
Контрольная работа №4 по теме «p-элементы» 10 класс
2 ВАРИАНТ
1. В ряду галогенов с возрастанием атомного номера:
| А) плотность простых веществ увеличивается, интенсивность окраски усиливается |
| Б) плотность уменьшается, интенсивность окраски усиливается |
| В) плотность увеличивается, интенсивность окраски ослабевает |
| Г) плотность веществ уменьшается, интенсивность окраски ослабевает |
2. Галогены в реакциях могут проявлять:
| А) только окислительные свойства |
| Б) только восстановительные свойства |
| В) окислительные и восстановительные свойства |
| Г) галогены не проявляют окислительно-восстановительные свойства |
Выберите правильный ответ.
3. Степень окисления +4 сера имеет в составе:
| А) Al2(SO4)3 | Б) Na2SO3 | В) Ca(HCO3)2 | Г) K2S |
4. Укажите формулы веществ, в состав которых входит сера проявляет свою максимальную степень окисления:
| А) FeS2 | Б) H2SO4 | В) SO2 | Г) SO3 |
5. Укажите схемы осуществимых реакций с участием сероводородной кислоты:
| А) K2S + H2S → | Б) H2S + KCl → | В) H2S + CuSO3 → | Г) KHS + H2S → |
6. С помощью, каких веществ можно обнаружить в растворе сульфат-ион?
| А) хлорид бария | Б) хлорид калия | В) нитрат серебра (I) | Г) нитрат натрия |
7. При определенных условиях концентрированная серная кислота реагирует с:
| А) железом | Б) нитратом натрия | В) ортофосфатом кальция | Г) оксидом меди (II) |
8. Концентрированная серная кислота, в отличие от разбавленной серной кислоты:
| А) при обычных условиях реагирует с железом и алюминием |
| Б) вытесняет из кристаллических хлоридов хлороводород |
| В) является окислителем за счет ионов H+ (Н3О+) |
| Г) является окислителем за счет ионов S6+ (SO42-) |
9. Азот и фосфор:
| А) находятся в одном периоде | Б) находятся в одной группе |
| В) находятся в разных подгруппах | Г) имеют одинаковое строение |
10. Азот в составе аммиака является:
| А) только окислителем | Б) только восстановителем |
| В) и окислителем, и восстановителем | Г) донором электронов |
11. Для определения нитрат-ионов необходимо взять:
| А) соль свинца | Б) соль серебра | В) ионы медь | Г) ионы золота |
12. Фосфор является восстановителем, реагируя с:
| А) магнием | Б) бертолетовой солью | В) хлором | Г) серой |
13. Чему равны валентность и степень окисления фосфора в H3PO4?
| А) III и +3 | Б) V и +3 | В) III и +5 | Г) V и +5 |
14. С каким веществом не реагирует H3PO4, но реагирует HNO3 разб?
| А) карбонатом калия | Б) оксидом кальция | В) медью | Г) карбонатом аммония |
15. Сколько аллотропных видоизменений образует углерод?
16. Поглощение поверхностью твердого вещества газов или растворимых веществ называется:
| А) регенерацией | Б) возгонкой | В) адсорбцией | Г) дистилляцией |
17. Отметьте схемы реакций, в результате которых выделяется оксид углерода (IV):
| А) Na2CO3 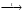 | Б) NaHCO3 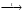 | В) CaCO3 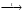 | Г) CaCO3 + HCl |
18. При обработке карбоната металла кислотой образуется:
| А) С (тв.) | Б) О2 (г) | В) СО (г) | Г) СО2 (г) |
19. В реакциях с азотом, углеродом и серой кремний проявляет свойства:
| А) окислителя | Б) восстановителя в реакции с азотом, окислителя в реакциях с серой и углеродом |
| В) восстановителя | Г) окислителем в реакции с углеродом, восстановителя в реакциях с азотом и серой |
20. Состав оконного стекла выражается формулой:
| А) Na2O·CaO·6SiO2 | Б) Mg3H4Si2O9 | В) CaAl2Si2O8 | Г) Al2O3·2SiO2·2H2O |
21. Масса серной кислоты, содержащаяся в 500 мл 0,2 М раствора
| A) 4,9 г | B) 9,8 г | C) 14,7 г | D) 19,6 г | E) 24,5 г |