
Добрый день!
Пусть сегодня для нас всех.
На урок придет успех!
Я желаю вам удачи,
И успешности в придачу!

С давних времен люди использовали приправы для придания пище кислого вкуса. С этой целью использовались яблоки, листья щавеля, сок лимона. Разумеется, тогда никто и не думал о том, что кислый вкус во всех случаях обусловлен присутствием соединений одного класса.
Какого?

Блицопрос
- 1. Какую кислоту используют для консервирования и маринования?
- Ответ. Уксусную кислоту.
- 2. Какую кислоту используют для приготовления компотов и напитков?
- Ответ. Яблочную кислоту.
- 3. Какую кислоту содержат молочнокислые продукты?
- Ответ. Молочную кислоту.
- 4. Об образовании какой кислоты свидетельствуют прогорклый вкус и специфический запах масла?
- Ответ. Масляной кислоты.
- 5. Какая кислота необходима для повышения набухаемости белков при приготовлении слоеного теста?
- Ответ. Лимонная кислота.
- 6. Что за кислота ежедневно образуется в организме человека в количестве 400 г?
- Ответ. Уксусная кислота.
- 7. Как по-другому называется метановая кислота?
- Ответ. Муравьиная кислота.
- 8. Почему болят икры ног после продолжительного бега?
- Ответ. В мышцах образуется молочная кислота.
- 9. Какая кислота содержится в янтаре?
- Ответ. Янтарная кислота.
- 10. Какие кислоты содержатся в табачном дыме?
- Ответ. Муравьиная и уксусная кислоты.

Дать название веществам
1. СН 3 - СН 2 - СН 2 – СН – СН – СООН
l l
СН 3 СН 3
2,3 – диметилгексановая кислота
СН 3 СН 3
l l
2. СН 3 - СН – С – СООН
l
СН 3
2,2,3 – триметилбутановая кислота
3. CH 3 – CH - COOH
׀
CH 3
2 – метилпропановая кислота

Дать название веществам
4. СН 3 – СН 2 –СН 2 – СН - СООН
l
СН 3
2 – метилпентановая кислота
СН 3 СН 3
l l
5. СН 3 - СН – СН – СООН
2,3 – диметилбутановая кислота
6. CH 3 – CH 2 – СН 2 - COOH
бутановая кислота

Уксусная кислота
С Н 3 – СООН
Водные растворы широко используются в пищевой промышленности (пищевая добавка E260) и бытовой кулинарии, а также в консервировании. Ежедневно образуется в организме человека в количестве 400 г?

В зависимости от природы углеводородного радикала карбоновые кислоты делятся на предельные, непредельные, ароматические.
Карбоновые кислоты, содержащие две карбоксильные группы, называются двухосновными .
Молекулы карбоновых кислот образуют димеры, в которых две молекулы кислоты связаны водородными связями .
Соли муравьиной кислоты называются ацетаты, а уксусной формиаты.
На дачном участке можно найти щавелевую кислоту.
Будет ли взаимодействовать уксусная кислота с жемчугом?

«Пир Клеопатры» 1653
“ Она … опустила жемчужину в уксус… Когда от нее не осталось и следа, Клеопатра подняла кубок, и выпила весь до последней капли”

Девиз урока:
« Зная строение вещества, можно предсказать его свойства»
А.М. Бутлеров.
Химические свойства карбоновых кислот
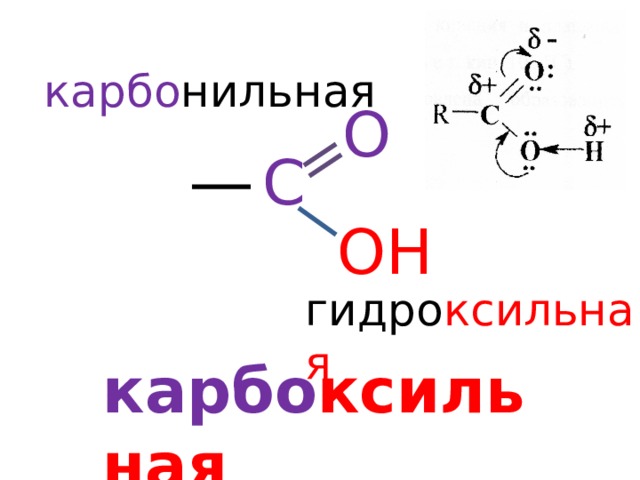
карбо нильная
О
С
ОН
гидро ксильная
карбо ксильная
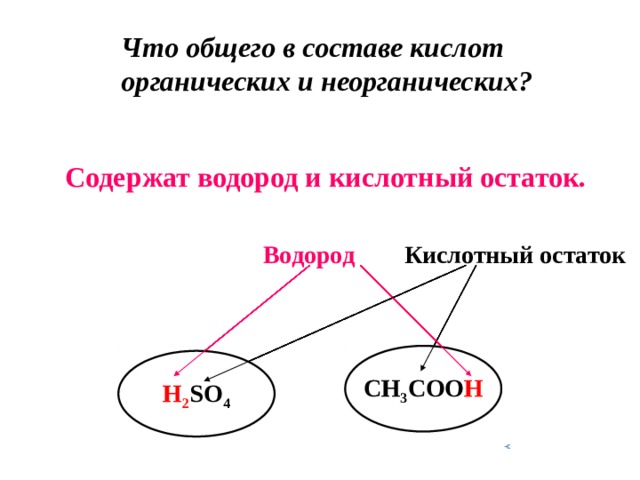
Что общего в составе кислот органических и неорганических?
Содержат водород и кислотный остаток.
Водород Кислотный остаток
CH 3 COO H
CH 3 COO H
CH 3 COO H
H 2 SO 4
H 2 SO 4
H 2 SO 4

Лабораторный опыт 18 Взаимодействие карбоновых кислот с металлами, основными оксидами, основаниями и солями
Группа 1. Взаимодействие с металлами и действие на индикатор
Группа 2. Взаимодействие с оксидами металлов, основаниями и солями слабых кислот

Правила техники безопасности
Будьте осторожны при работе с кислотами и щелочами! Внимательно прочитайте правила техники безопасности при работе с кислотами и щелочами, оборудованием и спиртовкой. Не допускайте попадания веществ на кожу и одежду!
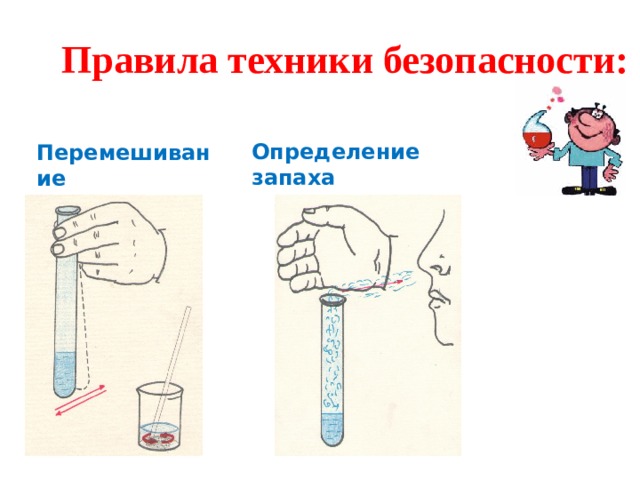
Правила техники безопасности:
Перемешивание
Определение запаха
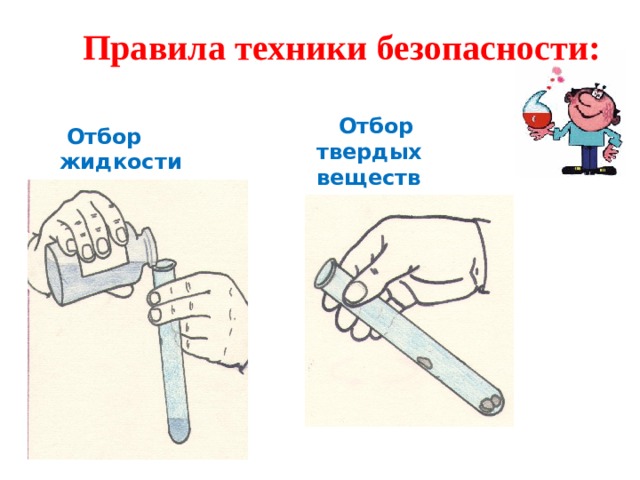
Правила техники безопасности:
Отбор твердых веществ
Отбор жидкости
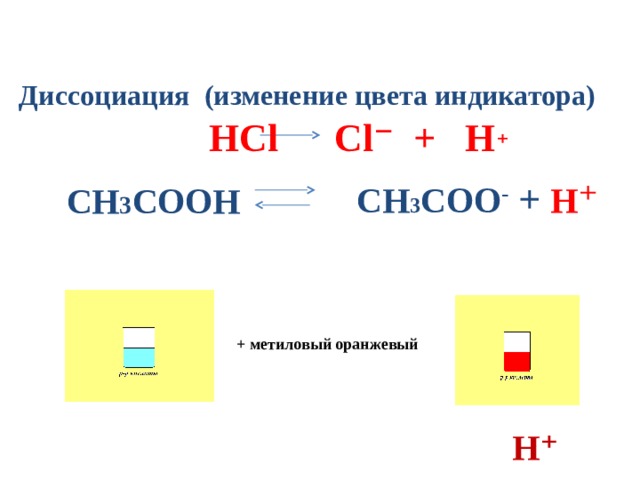
Диссоциация (изменение цвета индикатора)
НСl Сl⁻ + Н ⁺
СН 3 СОО - + Н ⁺
СН 3 СООН
+ метиловый оранжевый
Н⁺
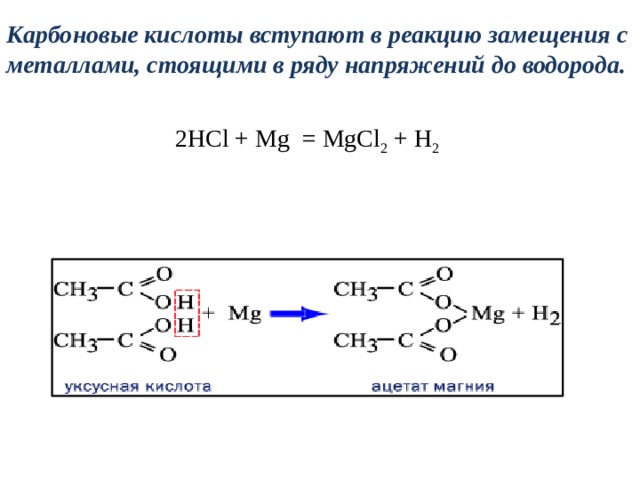
Карбоновые кислоты вступают в реакцию замещения с металлами, стоящими в ряду напряжений до водорода.
2НСl + Mg = MgCl 2 + H 2
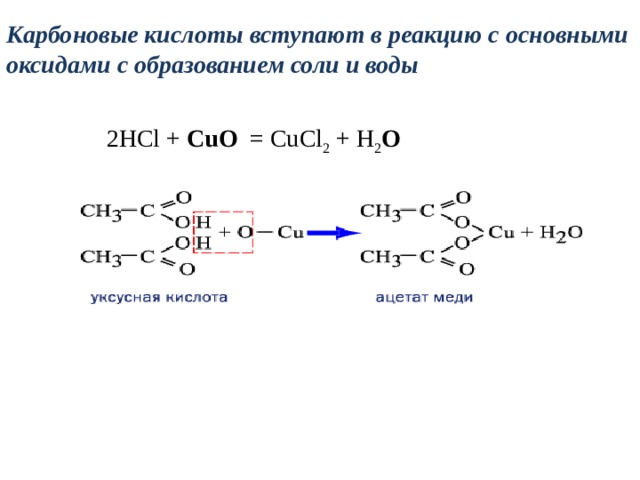
Карбоновые кислоты вступают в реакцию с основными оксидами с образованием соли и воды
2НСl + CuO = CuCl 2 + H 2 O
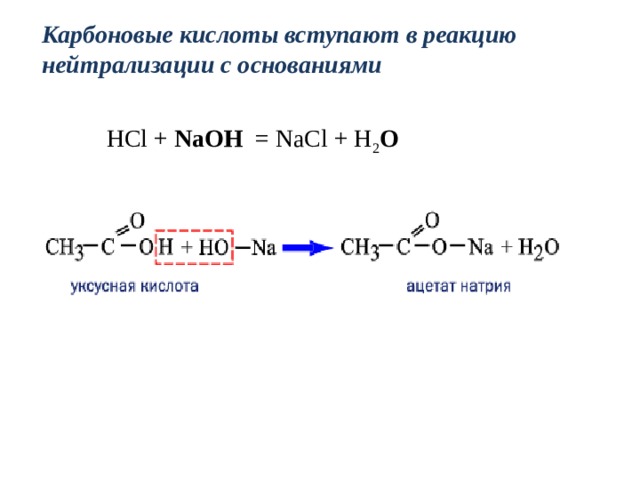
Карбоновые кислоты вступают в реакцию нейтрализации с основаниями
НСl + NaOH = NaCl + H 2 O
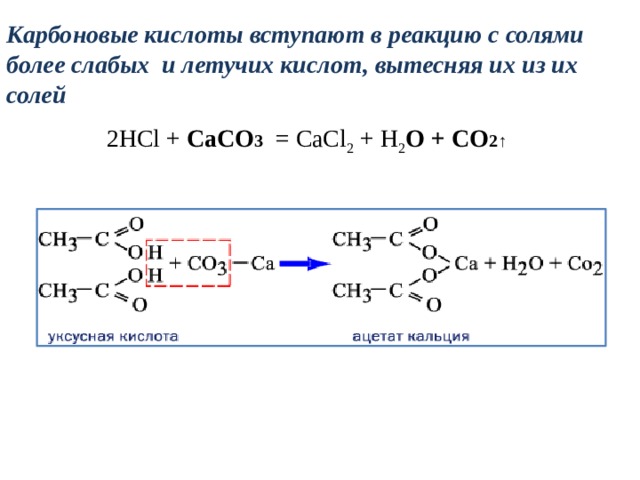
Карбоновые кислоты вступают в реакцию с солями более слабых и летучих кислот, вытесняя их из их солей
2НСl + CaCO 3 = CaCl 2 + H 2 O + CO 2↑

Слайды 19
Какую реакцию осуществила Клеопатра?
2СН 3 СООН + СаСО 3 = (СН 3 СОО) 2 Сa + H 2 O +CO 2 ↑

Домашнее задание:
Для всех обучающихся:
П. 20; № 6,7 (п.).
Задание по выбору
1.«Что скрывает буква Е- на этикетках?...» (Е-260, Е-200, Е-210). Составить краткое сообщение.
2.Решить задачу и дать мне совет.
Мне для консервирования нужно 300 г 3,5%-ного раствора СН3СООН. Какую массу 70%-ного раствора уксусной кислоты мне необходимо взять?
3.Составить кроссворд по теме «Химические свойства карбоновых кислот»

Рефлексия
Все отлично! Надо доработать Ещё работать и работать
















































