Просмотр содержимого документа
«Электролитическая диссоциация»
Электролитическая диссоциация
8класс
Неорганическая химия
Учитель химии ГБОУ ООШ п.Приморский Ахметвалиева Н.М.

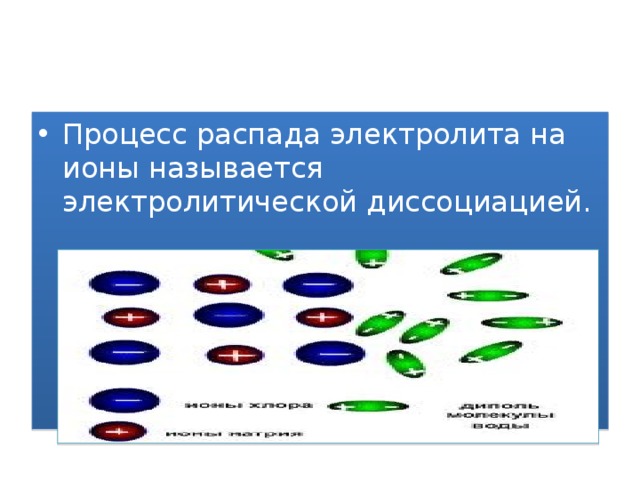
- Процесс распада электролита на ионы называется электролитической диссоциацией.
Вещества,
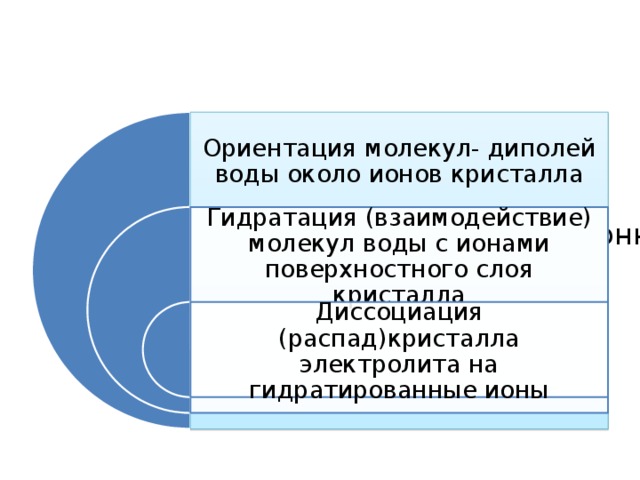
Ориентация молекул- диполей воды около ионов кристалла
Гидратация (взаимодействие) молекул воды с ионами поверхностного слоя кристалла
Диссоциация веществ с ионной связью
Диссоциация (распад)кристалла электролита на гидратированные ионы
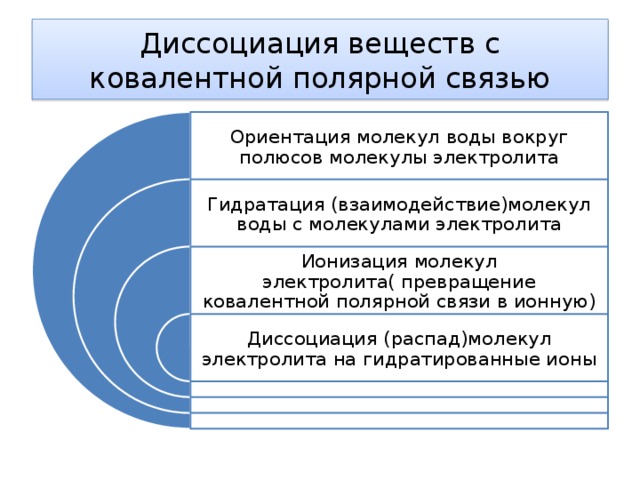
Диссоциация веществ с ковалентной полярной связью
Ориентация молекул воды вокруг полюсов молекулы электролита
Гидратация (взаимодействие)молекул воды с молекулами электролита
Ионизация молекул электролита( превращение ковалентной полярной связи в ионную)
Диссоциация (распад)молекул электролита на гидратированные ионы
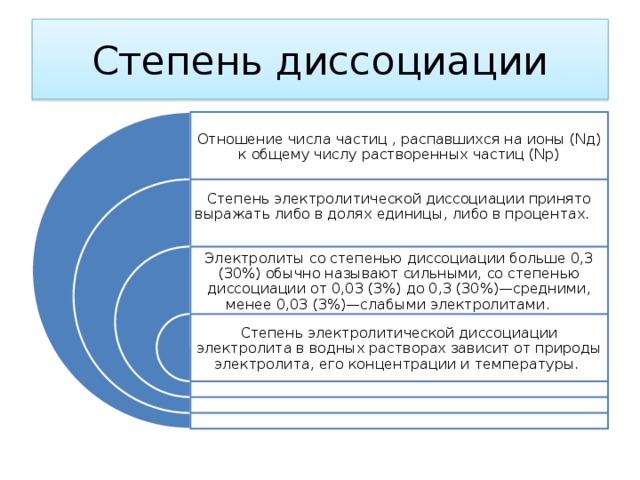
Степень диссоциации
Отношение числа частиц , распавшихся на ионы (Nд) к общему числу растворенных частиц (Np)
Степень электролитической диссоциации принято выражать либо в долях единицы, либо в процентах.
Электролиты со степенью диссоциации больше 0,3 (30%) обычно называют сильными, со степенью диссоциации от 0,03 (3%) до 0,3 (30%)—средними, менее 0,03 (3%)—слабыми электролитами.
Степень электролитической диссоциации электролита в водных растворах зависит от природы электролита, его концентрации и температуры.

Электролиты условно делятся:
- Сильные электролиты диссоциируют практически полностью (α = 1).
- Слабые электролиты диссоциируют на ионы в очень малой степени, в растворах они находятся, в основном в недиссоциированном состоянии (в молекулярной форме). Для слабых электролитов устанавливается равновесие между недиссоциированными молекулами и ионами.

К сильным электролитам относятся
1) кислоты (H 2 SO 4 , HCl, HNO 3 , HBr, HI, HClO 4 , HМnO 4 );
2 ) основания – гидроксиды металлов первой группы главной подгруппы (щелочи) – LiOH, NaOH, KOH, RbOH, CsOH, а также гидроксиды щелочноземельных металлов – Ba(OH) 2 , Ca(OH) 2 , Sr(OH) 2 ;.
3) соли, растворимые в воде

К слабым электролитам относятся:
- 1) неорганические кислоты (H 2 CO 3 , H 2 S, HNO 2 , H 2 SO 3 , HCN, H 3 PO 4 , H 2 SiO 3 , HCNS, HСlO и др.);
- 2) вода (H 2 O);
- 3) гидроксид аммония (NH 4 OH);
- 4) большинство органических кислот
- (например, уксусная CH 3 COOH, муравьиная HCOOH);
- 5) нерастворимые и малорастворимые соли и гидроксиды некоторых металлов

Тест по теме "Электролитическая диссоциация. Реакции ионного обмена"
- 1. К неэлектролитам относится:
- 1) нитрат калия 2) гидроксид бария 3) хлорид кальция 4) оксид азота(II)
- 2. К хорошо растворимым электролитам относится:
- 1) бромид натрия 2) гидроксид цинка 3) карбонат кальция 4) гидроксид магния
- 3. В водном растворе наибольшее количество сульфат-анионов образуется при
- диссоциации 1 моль:
- 1) Al 2 (SO 4 ) 3 2)PbS 3) CaSO 4 4) K 2 SO 4

Тест по теме "Электролитическая диссоциация
- 4. Катионы металла и анионы кислотного остатка образуютя при диссоциации:
- 1) оксидов 2) кислот 3) солей 4) оснований
- 5. Выберите верную запись правой части уравнения диссоциации карбоната калия:
- 1) = K + + CO 3 ¯ 2) = K + + CO 3 2- 3) = 2K + + CO 3 2- 4) = 2K + + HCO 3 ¯
- 6. Наибольшее количество анионов образуется при диссоциации 1 моль:
- 1) AlCl 3 2) Zn(OH) 2 3) Al(OH) 3 4) Zn(NO 3 ) 2

Использованные материалы:
www.edu.murmansk.ru/www/to_teacher/gia/chemistry/.../ted.doc
a-nomalia.narod.ru/100otkr/28.htm
О.С.Габриелян Химия.8 класс М., Дрофа,2010






































