
Аминокислоты. Белки

Определение аминокислот
Аминокислоты – это азотсодержащие органические вещества, в молекулах которых содержатся одновременно аминогруппа - NH 2 и карбоксильная группа – СООН
Следовательно, аминокислоты – это амфотерные органические соединения
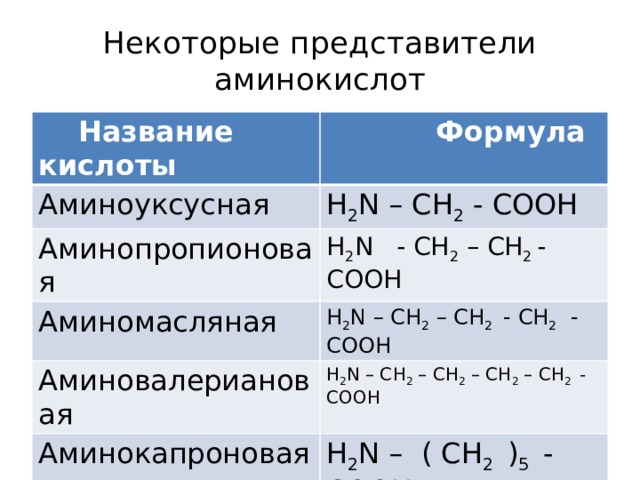
Некоторые представители аминокислот
Название кислоты
Формула
Аминоуксусная
H 2 N – CH 2 - COOH
Аминопропионовая
H 2 N - CH 2 – CH 2 - COOH
Аминомасляная
H 2 N – CH 2 – CH 2 - CH 2 - COOH
Аминовалериановая
H 2 N – CH 2 – CH 2 – CH 2 – CH 2 - COOH
Аминокапроновая
H 2 N – ( CH 2 ) 5 - COOH
Аминоэнантовая
H 2 N - ( CH 2 ) 6 - COOH

Изомерия аминокислот
Чем больше атомов углерода в молекуле аминокислоты, тем больше может существовать изомеров с различным положением аминогруппы по отношению к карбоксильной группе.
Изомерия аминокислот может быть обусловлена также разветвлением углеродного скелета

Номенклатура аминокислот
Чтобы в названиях изомеров можно было указывать положение аминогруппы по отношению к карбоксилу, атомы углерода в молекуле аминокислоты обозначают последовательно буквами греческого алфавита: γ β α
CH 3 – CH 2 – CH (NH 2 ) – COOH
α –аминомасляная кислота

Распространение в природе
Аминокислоты широко распространены в природе. Подобно тому как молекулы глюкозы – строительный материал для высокомолекулярных природных углеводов - крахмала и целлюлозы, молекулы аминокислот – это те кирпичики, из которых построены все растительные и животные белки. Разница лишь в том, что для крахмала и целлюлозы мономером служит одно вещество – глюкоза, а в состав каждого белка входят различные аминокислоты.
Встречаются аминокислоты в природе и в свободном виде, и в составе других соединений.

Физические свойства аминокислот
Аминокислоты представляют собой бесцветные кристаллические вещества, плавящиеся с разложением при температуре выше 200 0 С.
Они растворимы в воде и в зависимости от состава радикала могут быть сладкими, горькими или безвкусными.

Химические свойства аминокислот
1) Как кислоты, они реагируют с основаниями, образуя соли, например:
H 2 N – CH 2 –COOH + NaOH H 2 N-CH 2 COONa +
H 2 O
2) Как карбоновые кислоты, они взаимодействуют со спиртами, образуя сложные эфиры:
H 2 N-CH 2 -COOH + CH 3 OH H 2 N-CH 2 -COO-CH 3 + H 2 O
3) Как основания, они реагируют с кислотами, образуя соли:
H 2 N-CH 2 -COOH + HCl H 2 N-CH 2 -COOH + Cl -

Особое свойство аминокислот
Так как кислотные и основные свойства в аминокислотах представлены разными группами атомов, их молекулы могут реагировать друг с другом, например:
H 2 N-CH 2 CO OH + H 2 N -CH 2 -COOH
H 2 N-CH 2 - CONH -CH 2 COOH + H 2 O
Группа атомов СОNH, образующаяся при взаимодействии молекул аминокислот, называется пептидной или амидной группой, а связь между атомами углерода и азота в ней – пептидной ( амидной ) связью. Посредством пептидных связей аминокислотные остатки соединены друг с другом в молекулах белка.
Применение аминокислот
Питание
Лечение
Волокна
- человека животных
- человека
- животных
- Нервной системы Язвы желудка
- Нервной системы
- Язвы желудка
- Капрон Энант
- Капрон
- Энант
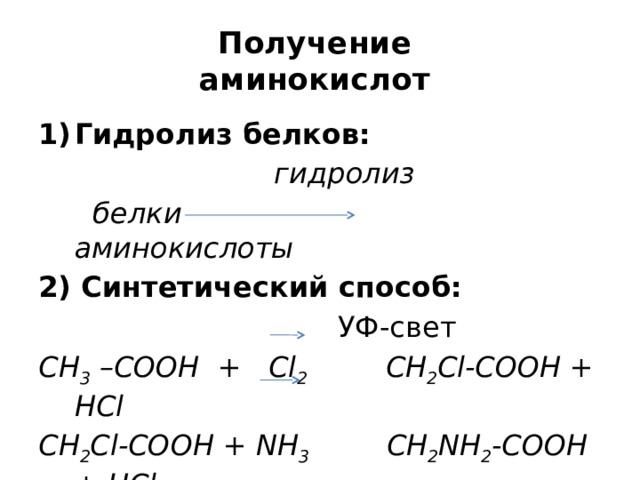
Получение аминокислот
гидролиз
белки аминокислоты
2) Синтетический способ:
УФ-свет
CH 3 –COOH + Cl 2 CH 2 Cl-COOH + HCl
CH 2 Cl-COOH + NH 3 CH 2 NH 2 -COOH + HCl

Состав и строение белков
Установлено, что в результате гидролиза любого белка получается смесь α- аминокислот , причем наиболее часто встречаются в составе белков 20 незаменимых аминокислот. Порядок чередования остатков аминокислот в полипептидной цепи определяет первичную структуру белка. Характеристика трех структур белковых молекул дана в таблице 4 на стр. 129 учебника.
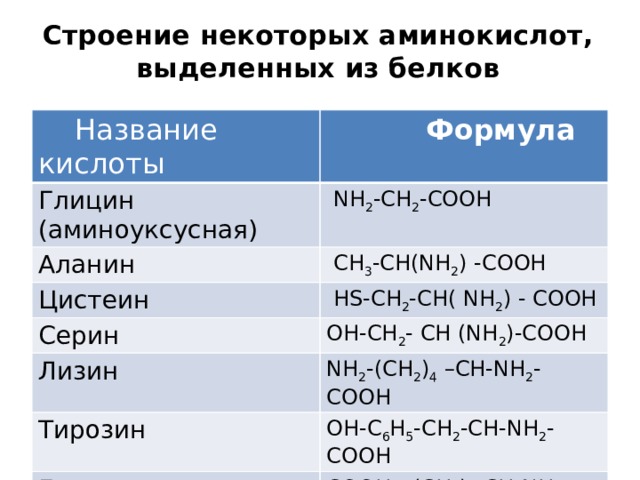
Строение некоторых аминокислот, выделенных из белков
Название кислоты
Формула
Глицин (аминоуксусная)
NH 2 -CH 2 -COOH
Аланин
СH 3 -CH(NH 2 ) -COOH
Цистеин
HS-CH 2 -CH( NH 2 ) - COOH
Серин
OH-CH 2 - CH (NH 2 )-COOH
Лизин
NH 2 -(CH 2 ) 4 –CH-NH 2 -COOH
Тирозин
OH-C 6 H 5 -CH 2 -CH-NH 2 - COOH
Глутаминовая
COOH- (CH 2 ) 2 -CH-NH 2 -COOH
Фенилаланин
С 6 H 5 -CH 2 -CH-NH 2 -COOH

Лабораторная работа «Свойства белков»
Оборудование и реактивы:
- Раствор белка куриного яйца;
2) NaOH – раствор щелочи;
3)Cu(SO 4 ) –раствор медного купороса (сульфата меди (II);
4) HNO 3( конц.) – азотная кислота
5)NH 4 OH –раствор аммиака (нашатырный спирт)
6) Сухое горючее

Биуретовая реакция
- В пробирку налейте 2 мл раствора белка и добавьте 2 мл раствора щелочи, а затем несколько капель раствора медного купороса (сульфата меди (II).
Что наблюдаете?
Это качественная реакция на белок.

Ксантопротеиновая реакция
2. В пробирку с 2 мл раствора белка добавьте (ОСТОРОЖНО!) несколько капель азотной кислоты. Что наблюдаете?
Нагрейте (ОСТОРОЖНО!) содержимое пробирки.
Что наблюдаете?
Охладите смесь и добавьте к ней по каплям 2-3 мл нашатырного спирта.
Что наблюдаете?
Это качественная реакция на белок.

Качественное определение серы в белках
- Если поджечь шерстяную нитку или пучок волос, ощущается характерный запах «жженого рога». Этот запах в значительной степени определяется содержанием в белках серы.

Вывод
- Белки дают две качественные реакции
- Большинство белков при температуре, под действием солей тяжелых металлов свертываются, то есть денатурируют

Домашнее задание
- Параграф 19, учить конспект , письменные упражнения 10,11, стр. 134 учебника












































